题目内容
19.在金刚石、CS2、N2、C2H4、H2O2、金属Fe 等六种晶体中:(1)以非极性键结合的非极性分子是N2.
(2)通过非极性键形成的原子晶体是金刚石.
(3)含有极性共价键和非极性共价键的非极性分子是C2H4.
(4)固态和熔融状态下都能导电的晶体是金属Fe.
分析 不同非金属元素之间易形成极性共价键,分子的结构对称、正负电荷的中心重合,则为非极性分子,如果存在自由移动的离子和电子就能导电,以此来解答.
解答 解:(1)双原子单质分子是以非极性键结合的非极性分子,则N2是以非极性键结合的非极性分子,故答案为:N2;
(2)金刚石是通过非极性键形成的原子晶体,故答案为:金刚石;
(3)C2H4分子中含有C-H极性共价键和C-C非极性共价键的非极性分子,故答案为:C2H4;
(4)金属Fe中存在自由电子,所以固态和熔融状态下都能导电,故答案为:金属Fe.
点评 本题主要考查极性键和非极性键,熟悉常见元素之间的成键是解答本题的关键,注意化学键、空间构型与分子的极性的关系来分析解答即可,难度不大.

练习册系列答案
相关题目
9.铝硅合金具有熔点低、凝固时收缩率小等优点,适合铸造.现取试样10.0mg,放在纯净氧气中完全燃烧,燃烧后的固体经称量发现比原来试样增重9.23mg,由此计算硅铝合金中硅的质量分数为( )
| A. | 12.3% | B. | 15.4% | C. | 13.4% | D. | 17.0% |
7.按碳骨架分类,下列说法正确的是( )
| A. | 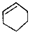 属于芳香族化合物 属于芳香族化合物 | B. | 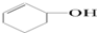 属于酚类化合物 属于酚类化合物 | ||
| C. | 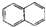 属于脂环化合物 属于脂环化合物 | D. | CH3CH(CH3)2属于链状化合物 |
14.下列各组物质熔点高低的比较正确的是( )
| A. | CF4>CCl4>CBr4>CI4 | B. | Na>Mg>Al | ||
| C. | SiO2>H2O>CO2 | D. | 晶体硅>SiC>金刚石 |
4.相同质量的下列各烃,完全燃烧后生成二氧化碳最多的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 乙炔 | D. | 乙烷 |
8.下列变化属于物理变化的是( )
| A. | 煤的干馏 | B. | 石油裂解 | ||
| C. | 蛋白质中加入饱和NH4Cl析出晶体 | D. | 古代植物变成煤 |