题目内容
【题目】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4- 、Fe(SCN)3 等。
(1)基态铁原子核外电子排布式为________________.
(2)科学研究表明用 TiO2 作光催化剂可将废水中 CN- 转化为OCN-,并最终氧化为 N2 、CO2。OCN- 中三种元素的第一电离能由大到小的顺序为_________。
(3)与 CN- 互为等电子体的一种分子为________________(填化学式);1mol Fe(CN)63- 中含有![]() 键的数目为________________。
键的数目为________________。
(4)铁的另一种配合物Fe(CO)5 熔点为 —20.5℃,沸点为 103℃,易溶于CCl4,据此可以判断Fe(CO)5 晶体属于________________(填晶体类型)。
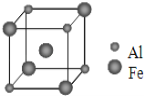
(5)铁铝合金的一种晶体属于体心立方结构,其晶胞可看成由 8 个小体心立方结构堆砌而成。已知小立方体如图所示,该合金的化学式为________________。
【答案】![]() 或[Ar]3d64s2 N>O>C CO或N2 12×6.02×10-23个或12NA 分子晶体 AlFe3
或[Ar]3d64s2 N>O>C CO或N2 12×6.02×10-23个或12NA 分子晶体 AlFe3
【解析】
(1)铁的原子序数为26,根据能量最低原理其态原子的电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2;
(2)同周期第一电离能自左而右具有增大趋势,所以第一电离能O>C.因为氮元素原子2p能级有3个电子,处于半满稳定状态,能量较低,第一电离能大于相邻元素,所以C、N、O三种元素的第一电离能由大到小的顺序是N>O>C;
(3)CN- 有2个原子,价电子数为10,可写出其等电子体为CO或N2,1个CN- 有1个![]() 键, CN- 与铁离子每形成一个配位键会增加一个
键, CN- 与铁离子每形成一个配位键会增加一个![]() 键,则1个Fe(CN)63-中
键,则1个Fe(CN)63-中![]() 键有12个,则1mol Fe(CN)63- 中含有
键有12个,则1mol Fe(CN)63- 中含有![]() 键的数目为12×6.02×10-23个;
键的数目为12×6.02×10-23个;
(4)Fe(CO)5 熔沸点较低,且易溶于有机物,可推测其为分子晶体;
(5)根据铁铝合金晶胞结构铝原子的数目为![]() ;铁原子数目为
;铁原子数目为![]() ,所以铝原子与铁原子个数之比为1:3,该铁铝合金的化学式为:AlFe3。
,所以铝原子与铁原子个数之比为1:3,该铁铝合金的化学式为:AlFe3。