题目内容
1.下列各组离子在指定条件下,能大量共存的是( )①在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
②使pH试纸变深蓝的溶液中:K+、CO32-、Na+、AlO2-
③水电离的c(H+)=10-13mol/L的溶液中:ClO-、CO32-、NO3-、NH4+、SO32-
④在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3-
⑤使甲基橙变红的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
⑥能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br-.
| A. | ①③ | B. | ①②⑤ | C. | ②⑤ | D. | ③⑥ |
分析 ①在含大量Fe3+的溶液中不能大量存在和铁离子反应的离子;
②使pH试纸变深蓝的溶液呈强碱性,不能大量存在和氢氧根离子反应的离子;
③水电离的c(H+)=10-13mol/L的溶液呈酸性或碱性;
④在加入铝粉能产生H2的溶液为强碱性或为非强氧化性酸溶液;
⑤使甲基橙变红的溶液呈强酸性;
⑥能使碘化钾淀粉试纸变蓝的溶液具有强氧化性.
解答 解:①在含大量Fe3+的溶液中不能大量存在和铁离子反应的离子,Fe3+、SCN-发生络合反应而不能大量共存,故错误;
②使pH试纸变深蓝的溶液呈强碱性,不能大量存在和氢氧根离子反应的离子,这几种离子之间不反应且和氢氧根离子不反应,所以能大量共存,故正确;
③水电离的c(H+)=10-13mol/L的溶液呈酸性或碱性,强酸性条件下不能大量存在ClO-、CO32-、SO32-,强碱性条件下不能大量存在NH4+,故错误;
④在加入铝粉能产生H2的溶液为强碱性或为非强氧化性酸溶液,酸性条件下,硝酸根离子和铝反应生成氮氧化物而不是氢气,强碱性条件下不能大量存在NH4+、Fe2+,故错误;
⑤使甲基橙变红的溶液呈强酸性,离子之间不反应,所以能大量共存,故正确;
⑥能使碘化钾淀粉试纸变蓝的溶液具有强氧化性,S2-、Br-不能大量共存,故错误;
故选C.
点评 本题考查离子共存,为高频考点,侧重考查复分解、氧化还原反应、络合反应等知识点,明确离子性质及离子反应条件是解本题关键,注意限制性条件的挖掘和运用,题目难度不大.

练习册系列答案
相关题目
11.下列各组内的物质属于同系物的是( )
| A. | CH3CH3 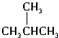 CH3CH2CH2CH2CH3 CH3CH2CH2CH2CH3 | |
| B. | CH3-CH3 CH2=CH-CH3 CH3CH=CHCH3 | |
| C. | 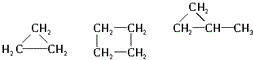 | |
| D. | CH3CH2CH2CH2CH3 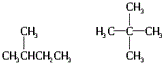 |
12.下列有关物质检验的实验结论正确的是( )
| 实 验 操 作 | 现 象 | 实 验 结 论 | |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| B | 将某气体通入澄清石灰水中 | 变浑浊 | 该气体一定是CO2 |
| C | 向某溶液中加入2滴KSCN溶液; | 溶液不显红色; | 溶液中一定含有Fe2+ |
| 另取样,先滴入氯水,再滴入KSCN溶液 | 溶液变为红色 | ||
| D | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| A. | A | B. | B | C. | C | D. | D |
6.标准状况下VL HCl气体溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,溶
质的质量分数为ω,物质的量浓度为c mol/L,溶质的质量为mg,则下列关系中不正确的是( )
质的质量分数为ω,物质的量浓度为c mol/L,溶质的质量为mg,则下列关系中不正确的是( )
| A. | m=$\frac{36.5V}{22.4}$ | B. | ω=$\frac{36.5c}{1000ρ}$ | ||
| C. | c=$\frac{1000ρV}{36.5V+22400}$ | D. | c=$\frac{V}{22.4+22.4V}$ |
13.下列仪器:①烧杯,②坩埚,③锥形瓶,④蒸发皿,⑤试管,⑥蒸馏烧瓶,⑦表面皿,用酒精灯加热时,须垫石棉网的是( )
| A. | ①⑥⑦ | B. | ②④⑤ | C. | ①③⑥ | D. | ③④⑥ |
11.100ml 6mol/L 硫酸与2g锌粒反应,在一定温度下为了减缓反应的速率,但又不影响生成氢气的总量,可向反应物中加入( )
| A. | 少量碳酸钠固体 | B. | 少量硫酸铜固体 | C. | 硝酸钾溶液 | D. | 氯化钠溶液 |
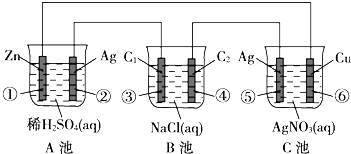 已知金属活动性相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题:(其中C1、C2都为石墨电极)
已知金属活动性相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题:(其中C1、C2都为石墨电极)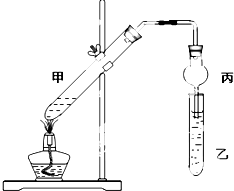
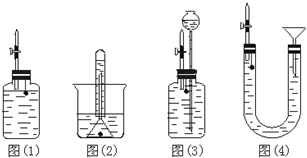 某研究型学习小组为测定镁和铝的混合物中铝的质量分数,称取该样品a g,溶于200mL 5mol/L HCl溶液中,共收集到标准状况下的氢气3.36L.
某研究型学习小组为测定镁和铝的混合物中铝的质量分数,称取该样品a g,溶于200mL 5mol/L HCl溶液中,共收集到标准状况下的氢气3.36L.