题目内容
2.在实验室中,下列除去杂质的方法正确的是( )| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取溴 | |
| B. | 硝基苯中混有浓硝酸和浓硫酸,将其倒入NaOH溶液中振荡,静置,分液 | |
| C. | 乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 | |
| D. | 乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液中洗气 |
分析 A.溴氧化KI生成碘,易溶于苯,且汽油与苯混溶;
B.硝基苯与氢氧化钠溶液不反应,可用碱中和酸;
C.乙烯含量不同确定,易引入新杂质;
D.乙烯被酸性高锰酸钾氧化.
解答 解:A.溴氧化KI生成碘,易溶于苯,且汽油与苯混溶,应加入氢氧化钠溶液除杂,故A错误;
B.硝基苯与氢氧化钠溶液不反应,可用碱中和酸,可除去杂质,故B正确;
C.乙烯含量不同确定,易引入新杂质,且在实验室难以完成该反应,故C错误;
D.乙烯可被氧化,应用氢氧化钠溶液除杂,故D错误.
故选B.
点评 本题综合考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,除杂时不能引入新的杂质,更不能影响被提纯物质的性质,难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
12.在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定表明化学平衡移动的是( )
| A. | 反应物的转化率 | B. | 反应体系的压强 | ||
| C. | 正、逆反应的速率 | D. | 反应混合物的浓度 |
13.锂硫电池的总反应式为2Li+S$?_{充电}^{放电}$Li2S,放电时,正极参加反应的物质是( )
| A. | Li | B. | S | C. | Li2S | D. | Li和S |
10.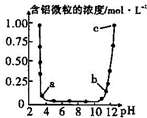 维持温度不变,向一定物质的量浓度的某AlCl3溶液中加入NaOH固体,忽略溶液体积的变化,溶液的pH与溶液中含铝微粒的物质的量浓度的关系如图.以下说法中正确的是( )
维持温度不变,向一定物质的量浓度的某AlCl3溶液中加入NaOH固体,忽略溶液体积的变化,溶液的pH与溶液中含铝微粒的物质的量浓度的关系如图.以下说法中正确的是( )
 维持温度不变,向一定物质的量浓度的某AlCl3溶液中加入NaOH固体,忽略溶液体积的变化,溶液的pH与溶液中含铝微粒的物质的量浓度的关系如图.以下说法中正确的是( )
维持温度不变,向一定物质的量浓度的某AlCl3溶液中加入NaOH固体,忽略溶液体积的变化,溶液的pH与溶液中含铝微粒的物质的量浓度的关系如图.以下说法中正确的是( )| A. | a点表示溶液中的Al3+开始转化为Al(OH)3沉淀 | |
| B. | 据图可知,配制一定物质的量浓度的AlCl3溶液时,需要加入适量的H2SO4溶液抑制水解 | |
| C. | 当溶液的pH在6至8之间,铝元素全部以Al(OH)3的形式存在 | |
| D. | b点所对应的溶液中主要含铝微粒的水解程度大于c点 |
17.下列气体中,室温下能大量共存的是( )
| A. | NH3、CO2、HCl | B. | H2、Cl2、H2S | C. | NH3、O2、H2 | D. | CO2、H2S、SO2 |
7.化学与社会、生活密切相关,对下列一些现象或事实的解释合理的是( )
| 选项 | 现象或事实 | 解释 |
| A | 热的纯碱溶液去油污效果 更好 | 温度升高,增大了油脂在碳 酸钠溶液中的溶解度 |
| B | 生活中的铝制品经久耐用 | 常温时铝不与氧气反应 |
| C | 氢氧化铁胶体通直流电,阴极颜色变深 | 氛氧化铁胶体带正电荷,在电场力的作用下,胶体向阴极迁移 |
| D | 二氧化破用作通讯光缆 | 二氧化硅对光信号有良好的 传输性能 |
| A. | A | B. | B | C. | C | D. | D |
16.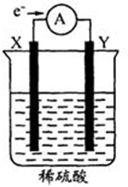 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.下列关于该装置的判断正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.下列关于该装置的判断正确的是( )
 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.下列关于该装置的判断正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.下列关于该装置的判断正确的是( )| A. | 外电路的电流方向为:X→导线→Y | |
| B. | 若两电极都是金属,则它们的活动性顺序为X>Y | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | 溶液中的SO42-向Y极移动 |
17.下列物质中,在一定条件下既能进行加成反应,也能进行取代反应,并且不能使KMnO4酸性溶液褪色的是( )
| A. | 乙烷 | B. | 乙烯 | C. | 乙醇 | D. | 苯 |