题目内容
17.下列气体中,室温下能大量共存的是( )| A. | NH3、CO2、HCl | B. | H2、Cl2、H2S | C. | NH3、O2、H2 | D. | CO2、H2S、SO2 |
分析 室温下氨气与氯化氢,氯气与硫化氢,硫化氢与二氧化硫能够相互反应,据此解答.
解答 解:A.氨气与氯化氢在常温下反应生成氯化铵,不能大量共存,故A错误;
B.氯气与硫化氢常温下发生氧化还原反应,生成硫和氯化氢,不能大量共存,故B错误;
C.NH3、O2、H2三种气体室温下相互不反应,可以共存,故C正确;
D.二氧化硫与硫化氢常温下发生氧化还原反应,不能共存,故D错误;
故选:C.
点评 本题考查了物质的性质,熟悉常见气体的性质是解题关键,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
8.在电治铝的电解槽中存在电解质W2[X2Y2Z4],己知四种元素的简单离子的电子层结构均相同,Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半,下列说法正确的是( )
| A. | 原子序数:W>X>Y>Z | |
| B. | 原子半径:W>X>Y>Z | |
| C. | W的最高价氧化物的水化物碱性比X的弱 | |
| D. | Y的简单氢化物的稳定性比Z的强 |
5.硼烷氨的化学式为H6NB,它是乙烷的等电子体,结构与乙烷类似.硼烷氨是最基本的硼氨化合物,因为氢经济的发展,硼烷氨因其稳定的储氢能力引起人们关注.下列有关硼烷氨的说法中正确的是( )
| A. | 原子半径:B<N | |
| B. | 硼烷氨分子与乙烷分子结构相似,分子内既含有极性共价键又含有非极性共价键 | |
| C. | 硼烷氨分子中的每个原子均达到最外层8电子稳定结构 | |
| D. | 硼烷氨分子中所有的H原子不可能在同一个平面内 |
12.下列化合物的同分异构体数目与C3H8O的同分异构体数目相同的是( )
| A. | C3H6 | B. | C5H12 | C. | C6H4Cl2 | D. | C4H8 |
2.在实验室中,下列除去杂质的方法正确的是( )
| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取溴 | |
| B. | 硝基苯中混有浓硝酸和浓硫酸,将其倒入NaOH溶液中振荡,静置,分液 | |
| C. | 乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 | |
| D. | 乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液中洗气 |
9.K2Fe04是一种既能杀菌消毒,豕能聚凝净水的水处理剂,工业上制备该物质的反应为:Fe(OH)3+C1O-+OH-→FeO42-+Cl-+H20 (未配平),则下列有关说法正确的是( )
| A. | 该物质作净水处理剂与Cl2的作用原理完全相同 | |
| B. | 该反应表明碱性条件下ClO-氧化性强于FeO42- | |
| C. | 上述反应中Fe(0H)3与ClO-的物质的量之比应为3:2 | |
| D. | 因为FeO32-可直接水解生成氢氧化铁胶体,故可做自来水的聚凝剂 |
11.运用元素周期律分析下面推断,其中错误的是( )
| A. | 硫酸锶(SrSO4)是难溶于水的白色固体 | |
| B. | 砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于酸 | |
| C. | 硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 | |
| D. | 铍(Be)的氧化物的水化物可能具有两性 |
12.碳碳双键不能自由旋转,所以,R-CH=CH-R可能有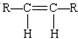 和
和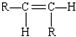 两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )
两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )
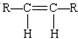 和
和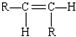 两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )
两种空间排列的形成,那么,下列化合物具有上述两种空间排列形成的是( )| A. | 丙烯 | B. | 2-戍烯 | C. | 苯乙烯 | D. | 1,3-丁二烯 |