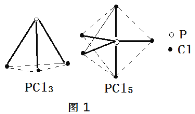
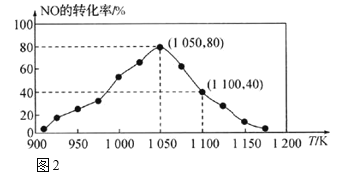
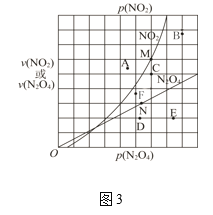
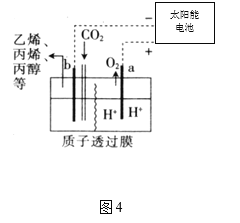
题目内容
【题目】某化工厂生产新型清洁燃料甲醚(CH3-O-CH3)的流水线反应原理为:在 10L 的反应容器内进行的反应①的化学平衡常数表达式为K=[CO][H2]/[H2O]。反应②的热化学方程式为:3H2(g)+3CO(g)CH3OCH3(g)+CO2(g)+Q。反应③为:CO2+NH3+H2O→NH4HCO3,完成下列填空:
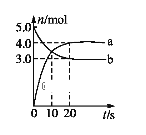
(1)反应①的方程式为______。经3min反应容器内的水蒸气从20.0mol变为 2.0mol,则此 3min 内 CO 的平均反应速率V(CO)=______。
(2)能判断反应①已达化学平衡状态的是(选填编号)______。
A.在消耗 n 摩尔氢气的同时产生 n 摩尔的水
B.容器内气体的平均相对分子质量保持不变
C.容器内所有的物质的总物质的量保持不变
D.化学反应速率:V(逆)(H2O)=V(正)(CO)
(3)已知升高温度,反应②的化学平衡常数会减小,则反应②的热化学方程式中的Q(选填“>”或“<”)______0。该反应的逆反应速率V(逆)随时间 t 变化的关系如图一所示,则在 t2时改变的反应条件是______。
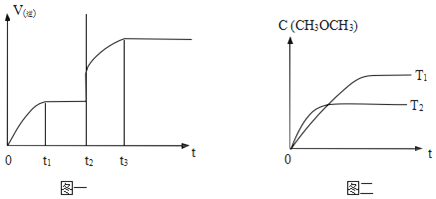
(4)在不同温度下,反应容器内甲醚(CH3OCH3)的浓度c(CH3OCH3)随时间t 变化的状况如图二所示。则反应温度 T1(选填“>”、“=”或“<”)______T2。
(5)若反应③得到的是一种纯净常见化肥的溶液。经测定溶液中也存在 NH3H2O 分子和CO32-离子,试用化学用语表示产生这两种微粒的原因:______,______。相同温度下,都为 0.1mol/L的 NaHCO3溶液甲和 NH4HCO3溶液乙相比较,溶液中c(CO32-)甲(选填“>”、“=”或“<”)甲______乙。
【答案】C(s)+H2O(g)CO(g)+H2(g) 0.6mol/(Lmin) B、D > 增大压强(或压缩反应容器体积) < NH4HCO3=NH4++HCO3-,NH4++H2ONH3H2O+H+ HCO3-H++CO32 >
【解析】
(1)根据反应①的平衡常数表达式,CO和H2是生成物,H2O(g)是反应物,再由元素守恒配平方程式,根据v=![]() 计算化学反应速率;
计算化学反应速率;
(2)可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变;
(3)升高温度,反应②的化学平衡常数会减小,说明温度升高不利于反应正向进行,根据图象,t2时刻速率突然增大,并且不断增大,然后趋于平衡;
(4)温度升高,化学反应速率加快,到达平衡的时间缩短,据此判断;
(5)根据影响盐类水解的因素分析。
(1)根据反应①的平衡常数表达式可知CO和H2是生成物,H2O(g)是反应物,所以方程式为:C(s)+H2O(g)CO(g)+H2(g);经3min反应容器内的水蒸气从20.0mol变为2.0mol,即△n(H2O)=20.0mol-2.0mol=18mol,根据方程式,则△n(CO)=△n(H2O)=18mol,所以v(CO)=![]() =0.6mol/(Lmin),故答案为:C(s)+H2O(g)CO(g)+H2(g);0.6mol/(Lmin);
=0.6mol/(Lmin),故答案为:C(s)+H2O(g)CO(g)+H2(g);0.6mol/(Lmin);
(2)A.在消耗n摩尔氢气的同时产生n摩尔的水,整个反应过程都是如此,不能判断化学平衡,故A错误;
B.容器内气体的平均相对分子质量数值上=![]() ,反应前后气体m改变,n改变,所以容器内气体的平均相对分子质量改变,当其不变时可以说明化学平衡,故B正确;
,反应前后气体m改变,n改变,所以容器内气体的平均相对分子质量改变,当其不变时可以说明化学平衡,故B正确;
C.容器内所有的物质的总物质的量保持不变,由于整个反应前后,反应物和生成物的总物质的量始终不变,不可以说明化学平衡,故C错误;
D.反应到达平衡时,v正=v逆,则v(逆)(H2O)=v(正)(H2O),根据方程式可知v(正)(CO)=v(正)(H2O),所以v(逆)(H2O)=v(正)(CO)可以说明化学平衡,故D正确,
故答案为:B、D;
(3)升高温度,反应②的化学平衡常数会减小,说明温度升高不利于反应正向进行,正反应放热,所以Q>0;根据图象,t2时刻速率突然增大,并且不断增大,然后趋于平衡,可判断为增大压强(或压缩反应容器体积),
故答案为:>;增大压强(或压缩反应容器体积);
(4)温度升高,化学反应速率加快,到达平衡的时间缩短,则温度T2>T1,
故答案为:<;
(5)反应③得到的是一种纯净常见化肥的溶液,产生NH4HCO3,溶液中也存在NH3H2O分子和CO32-离子,为NH4+水解得到NH3,HCO3-电离得到CO32-,所以有:NH4HCO3=NH4++HCO3-,NH4++H2ONH3H2O+H+,HCO3-H++CO32-,相同温度下,都为0.1mol/L的NaHCO3溶液甲和NH4HCO3溶液乙相比较,由于双水解促进盐类水解,导致NH4HCO3中HCO3-进一步降低,则电离出更少的CO32-,则c(CO32-)甲>乙,
故答案为:NH4HCO3=NH

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】甲醇既是基本有机化工原料,又可作为燃料用于替代矿物燃料。
(1)工业上合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
平衡常数K | 2.041 | 0.270 | 0.012 |
由表中数据判断该反应为 ________反应(填“吸热”或“放热”)。 某温度下,将2 molCO和6 molH2充入2 L的密闭容器中充分反应,达到平衡后,测得c(CO)=0.2 mol/L,则CO的转化率为______,此时的温度为______(从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2kJ/mol
③H2O(g)=H2O(l) ΔH3kJ/mol
则反应CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH= _____________ kJ/mol(用ΔH1、ΔH2、ΔH3表示)。
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法:
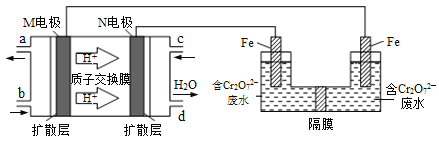
①N电极的电极反应式为 ___________________________________。
②请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:
Cr2O72 + ______ Fe2+ + ______ = ______ Cr3+ + ______ Fe3+ + ______
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×105 mol/L时,Cr3+沉淀完全,此时溶液的pH=______。(已知:Ksp=6.4×1031,lg2=0.3)
【题目】下列实验能达到实验目的是( )
序号 | 实验内容 | 实验目的 |
A | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向FeCl3+3KSCN | 说明增加生成物浓度,平衡逆向移动 |
C | 向盛有AgCl悬浊液的试管中滴加0.1mol·L-1NaI溶液,浊液变黄 | 证明相同温度下, KSP(AgCl)>KSP(AgI) |
D | 酸式滴定管中硫酸液面在20.00mL,将滴定管中液体全部放出 | 量取20.00mL硫酸溶液 |
A.AB.BC.CD.D