题目内容
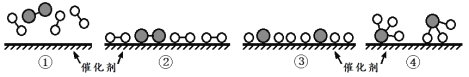
【题目】已知:Br+H2 HBr+H,其反应的历程与能量变化如图所示,以下叙述正确的是
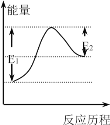
A.该反应是放热反应
B.加入催化剂,E1-E2的差值减小
C.H-H的键能大于H-Br的键能
D.因为E1>E2,所以反应物的总能量高于生成物的总能量
【答案】C
【解析】
根据反应物的总能量和生成物的总能量的相对大小来判断反应的热效应。反应的能量变化与反应途径无关,催化剂只改变反应速率,与该反应的能量变化无关。
A. 若反应物的总能量>生成物的总能量,则反应为放热反应;若反应物的总能量>生成物的总能量,则反应为吸热反应,此图中生成物总能量高于反应物,故该反应为吸热反应,A错误;
B. E1-E2的差值即为此反应的焓变,催化剂只改变活化能,与焓值无关,B错误;
C. 此反应为吸热反应,故断开H-H键所需要的能量高于生成H-Br键放出的能量,C正确;
D. 因为E1>E2,所以反应物的总能量低于生成物的总能量,此反应吸收热量,D错误,
故合理选项是C。

练习册系列答案
相关题目