题目内容
8.常温下,向20mL 0.005mol/L FeCl3溶液中加入20mL 0.1mol/L KSCN溶液,溶液呈红色.将该溶液平均分为4份,恒温下分别进行下列实验,其现象不正确的是( )| A. | 加入5.6g 铁粉充分反应后,溶液红色褪去 | |
| B. | 加入40mL水充分振荡后,静置,溶液红色变浅 | |
| C. | 加入10g Fe2(SO4)3固体充分反应后,溶液红色明显加深 | |
| D. | 加入20mL 0.001 mol/L KSCN溶液充分反应后,溶液红色明显变深 |
分析 A、依据Fe+2Fe3+=3Fe2+,平衡逆向进行,Fe3++3SCN-?Fe(SCN)3,红色退去;
B、加水稀释平衡Fe3++3SCN-?Fe(SCN)3,逆向进行微粒的浓度减小;
C、加入10g Fe2(SO4)3固体充分反应后,平衡正向进行;溶液颜色加深;
D、加入20mL 0.001 mol/L KSCN溶液充分反应后,SCN-浓度减小,溶液颜色变浅.
解答 解:A、依据发生的反应Fe+2Fe3+=3Fe2+,铁离子浓度减小平衡逆向进行,Fe3++3SCN-?Fe(SCN)3,溶液红色退去,故A正确;
B、加水稀释Fe3++3SCN-?Fe(SCN)3,平衡逆向进行,平衡状态下各微粒的浓度减小,静置,溶液红色变浅,故B正确;
C、加入10g Fe2(SO4)3固体充分反应后,Fe3+离子浓度增大,平衡正向进行,Fe(SCN)3浓度增大溶液颜色加深,故C正确;
D、加入20mL 0.001 mol/L KSCN溶液充分反应后,体积改变必平衡改变大,SCN-浓度减小,溶液颜色变浅,故D错误;
故选D.
点评 本题考查了化学平衡的影响因素分析判断,主要是铁离子检验的化学平衡的影响因素判断,溶液颜色变化和微粒浓度有关,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.某元素原子核内质子数为m,中子数为n,则下列论断正确的是( )
| A. | 这种元素的相对原子质量为m+n | |
| B. | 若碳原子质量为wg,则此原子的质量为(m+n)wg | |
| C. | 不能由此确定该元素的相对原子质量 | |
| D. | 核内中子的总质量小于质子的总质量 |
16. 已知某种气态化石燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收).
已知某种气态化石燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收).
根据实验数据求:
(1)实验完毕后,生成物中水的质量为1.8 g.假设广口瓶里生成一种正盐,其质量为5.0 g.
(2)生成的水中氢元素的质量为0.2 g.
(3)生成的CO2中碳元素的质量为0.6 g.
(4)气态化石燃料中碳元素与氢元素的质量比为3:1.
 已知某种气态化石燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收).
已知某种气态化石燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收).| 实验前 | 实验后 | |
| (干燥剂+U形管)的质量 | 101.1g | 102.9g |
| (石灰水+广口瓶)的质量 | 312.0g | 314.2g |
(1)实验完毕后,生成物中水的质量为1.8 g.假设广口瓶里生成一种正盐,其质量为5.0 g.
(2)生成的水中氢元素的质量为0.2 g.
(3)生成的CO2中碳元素的质量为0.6 g.
(4)气态化石燃料中碳元素与氢元素的质量比为3:1.
3.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A. | 分散质粒子直径都在10-9~10-7m之间 | |
| B. | 都能产生丁达尔效应 | |
| C. | 它们都属于混合物 | |
| D. | 颜色相同 |
13.对下列有机反应类型的认识中,错误的是( )
| A. | 苯乙烯使溴水褪色;加成反应 | |
| B. | 乙烯水化生成乙醇;取代反应 | |
| C. | 乙醇与CuO加热反应生成乙醛;氧化反应 | |
| D. | 无水乙醇与浓硫酸加热到170℃制取乙烯;消去反应 |
20.(1)短周期元素中原子核外p轨道上电子数与s轨道上电子总数相等的元素是O、Mg(写元素符号).
(2)Ti(BH4)2是一种重要的储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(3)H2S和H2O2的主要物理性质如表所示:
H2S和H2O2的相对分子质量基本相同,造成上述物理性质差异的主要原因是H2O2分子之间会形成氢键,熔沸点高,H2O2与水分子之间会形成氢键,溶解度大.
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为CN-或C22-(写出一个即可).
(5)已知CrO5中Cr为+6价,则CrO5的结构式为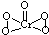 .
.
(2)Ti(BH4)2是一种重要的储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(3)H2S和H2O2的主要物理性质如表所示:
| 熔点/K | 沸点/K | 水中的溶解度(标准状况) | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为CN-或C22-(写出一个即可).
(5)已知CrO5中Cr为+6价,则CrO5的结构式为
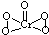 .
.
17.在H2SO3溶液中,在采取措施使c(H+)减小的同时,c(SO${\;}_{3}^{2-}$)的变化情况是( )
| A. | 增大 | B. | 减小 | ||
| C. | 不变 | D. | 可能增大也可能减小 |