题目内容
【题目】已知新型中温全瓷铁—空气电池,其结构简式如图所示。下列说法正确的是
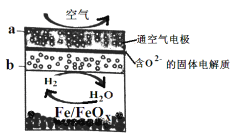
A. 铁表面发生的反应为 xH2O(g)+Fe=FeOx+xH2
B. a 极发生氧化反应
C. 正极的电极反应为 FeOx+2xe- =Fe+xO2-
D. 若有 22.4L(标准状况 )空气参与反应,则电路中有 4mol 电子转移
【答案】A
【解析】A、由新型中温全瓷铁-空气电池的装置图可知,铁表面发生失去电子的氧化反应,电极反应式为xH2O(g)+Fe=FeOx+xH2↑,A正确;B、a极空气中氧气得电子发生还原反应,B错误;C、a极空气中氧气得电子发生还原反应为正极,电极反应式为:O2+4e-=2O2-,C错误;D、有22.4L(标准状况)空气参与反应,则氧气为(22.4L÷22.4L/mol)×1/5=0.2mol,则电路中转移0.8mol电子,D错误;答案选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
A | B | C | D | |
实 | 用CCl4提取 | 除去乙醇中的苯酚 | 从KI和I2的固体 | 配制100mL 0.1000 |
装 |
|
|
|
|
A.A
B.B
C.C
D.D
【题目】在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:A(g)![]() B(g)+C(g) △H =+85.1kJ/mol 反应时间(t)与容器内总压强(P)的数据见下表:
B(g)+C(g) △H =+85.1kJ/mol 反应时间(t)与容器内总压强(P)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强P/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
计算平衡时A的转化率__________和平衡常数___________________。


