题目内容
19.100mL ρ=1.84g/cm3,质量分数为98%的浓硫酸中含H2SO4的物质的量是1.84mol,硫酸物质的量浓度是18.4mol/L.分析 根据n=$\frac{m}{M}$计算硫酸的物质的量,根据c=$\frac{1000ρw%}{M}$计算硫酸的物质的量浓度.
解答 解:100mL ρ=1.84g/cm3,质量分数为98%的浓硫酸中含H2SO4的物质的量是$\frac{100×1.84×98%}{98}$=1.84mol,硫酸物质的量浓度是$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L.
故答案为:1.84mol,18.4mol/L.
点评 本题考查物质的量浓度、物质的量的计算知识,注意公式的灵活应用是关键,难度中等.

练习册系列答案
相关题目
7.下列说法中,正确的是( )
| A. | 石油是混合物 | |
| B. | 油脂是天然高分子化合物 | |
| C. | 铜的活动性比铁弱,可在海轮外壳装铜块减缓海轮腐蚀 | |
| D. | 氨气显碱性,可用浓硫酸干燥 |
4.用NA表示阿伏加德罗常数的值,下列有关说法不正确的是( )
| A. | 标准状况下,22.4LN2与CO混合气体的质量为28g | |
| B. | 常温常压下,金属与酸反应生成2g H2,转移电子数为2NA | |
| C. | 含0.2NA个阴离子的Na2O2和水反应时,转移0.2mol电子 | |
| D. | 1L1mol•L-1的氨水,含NA个NH3•H2O |

 .
.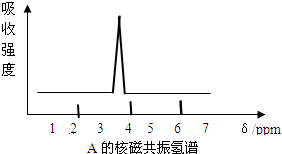 (1)按系统命名法命 (1)有机物CH3CH(C2H5)CH(CH3)2的名称是2,3-二甲基戊烷.
(1)按系统命名法命 (1)有机物CH3CH(C2H5)CH(CH3)2的名称是2,3-二甲基戊烷.