题目内容
18.下列元素中,原子半径最小的是( )| A. | Cl | B. | S | C. | P | D. | Si |
分析 同周期随原子序数增大,原子半径减小.
解答 解:Si、P、S、Cl同周期,核电荷数依次增大,原子核对核外电子吸引增大,原子半径减小,故原子半径:Si>P>S>Cl,故选:A.
点评 本题考查原子半径比较,比较基础,注意从结构理解同主族、同周期原子半径变化规律.

练习册系列答案
相关题目
8.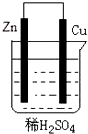 关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
 关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ③④⑥ |
6.下列说法中正确的是( )
| A. | 离子化合物中可能含有共价键 | |
| B. | 共价化合物中可能含有离子键 | |
| C. | 离子化合物中只含离子键 | |
| D. | 只含共价键的物质一定是共价化合物 |
13.设NA为阿伏加德罗常数的值.下列说法中,正确的是( )
| A. | 1mol Na被氧化完全转化生成Na2O2,失去电子数为2NA | |
| B. | 常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA | |
| C. | 将lmL 1 mol•L-1FeCl3溶液逐滴加入沸水,制得红褐色Fe(OH)3胶体,所含胶粒的数目是1×10-3NA | |
| D. | 标准状况下,6.72L NO2与足量水充分反应转移的电子数目为0.3NA |
10.常温时,下列说法中正确的是( )
| A. | 0.l mol/L醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 | |
| C. | 往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中$\frac{c(C{H}_{3}COOH)}{c({H}^{+}).c(C{H}_{3}CO{O}^{-})}$增大 | |
| D. | 含等物质的量浓度的CH3COOH和CH3COONa混合溶液中:2c(H+)-c(CH3COO-)=2c(OH-)-c(CH3COOH) |
7.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A. | 断开1 mol H-H的同时断开2 mol N-H | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | N2与H2的物质的量之和是NH3的物质的量2倍 | |
| D. | 单位时间里每增加1molN2,同时增加3molH2 |
8.配制一定物质的量浓度的K2SO4溶液时,造成最终浓度偏低的原因可能是( )
| A. | 容量瓶事先未烘干 | B. | 定容时观察液面仰视 | ||
| C. | 定容时观察液面俯视 | D. | 定容,摇匀后有少量液体流出 |