题目内容
3.设NA为阿伏加德罗常数,下列说法中正确的是( )| A. | 1000mL0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| B. | 2NA个二氧化碳分子的质量为44g | |
| C. | NA个氢气分子所占的体积为22.4L | |
| D. | 17g氨气中所含原子数为NA |
分析 A、n=c×V,据此计算微粒个数;
B、二氧化碳的摩尔质量为44g/mol,2NA个二氧化碳分子为2mol,依据m=n×M计算质量;
C、气体体积大小与压强和温度有关;
D、1个氨气中存在3个H原子和一个N原子.
解答 解:A、1000mL0.1mol/L 的NaCl溶液,氯化钠的物质的量=1L×0.1mol/L=0.1mol,氯化钠完全电离生成钠离子和氯离子.两者总数为0.2mol,故A正确;
B、2NA个二氧化碳分子的质量=2mol×44g/mol=88g,故B错误;
C、标况下,任何1mol气体的体积为22.4L,此题未说明气体所处的状态,故C错误;
D、17g氨气的物质的量未1mol,含有原子数为3+1=4mol,故D错误,故选A.
点评 本题考查了阿伏伽德罗常数的应用,主要考查阿伏伽德罗常数的规定,气体摩尔体积的条件应用,摩尔质量的概念判断,题目较简单.

练习册系列答案
相关题目
13.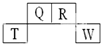 短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
 短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如下,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )| A. | H2R2的分子中既含有极性共价键,又含有非极性共价键 | |
| B. | T的氧化物是一种良好的半导体材料 | |
| C. | Q、R的简单氢化物分子所含质子数、电子数与Ne分子相同 | |
| D. | Q的氢化物与W的氢化物反应有白烟现象,且生成物中既含有离子键,又含有共价键 |
14.胶体区别于其它分散系最本质的特征是( )
| A. | 外观均一 | B. | 能发生丁达尔效应 | ||
| C. | 很稳定 | D. | 分散系粒子直径介于10-9m~10-7m |
8.设NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 1.7 g羟基所含有的电子数为NA | |
| B. | 标准状况下,11.2L苯含有的氢原子数为3NA | |
| C. | 28 g乙烯和环丙烷(C3H6)的混合气体中含有的碳原子数为2NA | |
| D. | 1mol乙醇和1mol乙酸和浓硫酸共热,充分反应后生成乙酸乙酯分子数为NA |
12.在t℃时,10L 0.4mol•L-1H2O2溶液发生催化分解:2H2O2═2H2O+O2↑,不同时刻测得生成O2的体积如下表,已知反应至6min时,H2O2分解了50%(已折算为标准状况)
下列叙述正确的是(溶液体积变化忽略不计)( )
| t/min | 0 | 2 | 4 | 6 |
| V(O2)/L | 0.0 | 9.9 | 17.2 | V=? |
| A. | 0~2min H2O2平均反应速率比4~6min慢 | |
| B. | 反应至6min时,共产生O244.8L | |
| C. | 0~6min的平均反应速率 v(H2O2)≈3.3×10-2mol•L-1•min-1 | |
| D. | 反应至6min时,c(H2O2)=0.3mol•L-1 |
13.下列有关化学反应及其分类的叙述不正确的是( )
| A. | 金属的冶炼、电镀、燃料的燃烧、食物的腐败、钢铁的锈蚀等均属于氧化还原反应 | |
| B. | 将铁片投入硫酸铜溶液中所发生的置换反应既属于氧化还原反应,又属于离子反应 | |
| C. | 有单质参与的化学反应一定是氧化还原反应 | |
| D. | 氧化还原反应一定发生电子转移 |
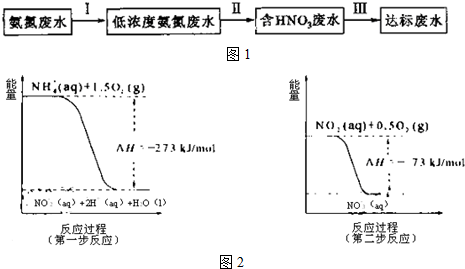
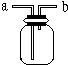 如图所示是中学化学实验中常见的装置,它有多种用途.
如图所示是中学化学实验中常见的装置,它有多种用途.