题目内容
【题目】如图为阳离子交换膜法以石墨为电极电解饱和食盐水原理示意图.据图判断下列说法不正确的是( ) 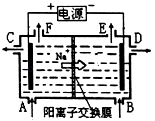
A.标准状况下,生成22.4LCl2的同时有2molNaOH生成
B.从C口流出的是NaOH溶液
C.从E口逸出的气体是H2
D.从F口逸出的气体是Cl2
【答案】B
【解析】解:A.电解原理方程式2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑,标准状况下每生成22.4L即1molC12 , 便产生2molNaOH,故A正确; B.阳离子交换膜仅允许Na+通过,则在C口不可能有NaOH导出,故B错误;
2NaOH+Cl2↑+H2↑,标准状况下每生成22.4L即1molC12 , 便产生2molNaOH,故A正确; B.阳离子交换膜仅允许Na+通过,则在C口不可能有NaOH导出,故B错误;
C.在电解池中,钠离子移向阴极,所以D极是阴极,发生2H++2e﹣=H2↑,故从E口逸出的气体是H2 , 故C正确;
D.左侧电极阳极,溶液中的阴离子氯离子失电子生成氯气,电极反应为:2Cl﹣﹣2e﹣=Cl2↑,故D正确;
故选B.
由电源正负极可知左侧电极为阳极,发生:2Cl﹣﹣2e﹣=Cl2↑,则右侧电极为阴极,发生2H++2e﹣=H2↑,电解时,阳极生成氯气,消耗NaCl,则应在阳极补充NaCl,阴极生成OH﹣ , 且Na+向阴极移动,则产品烧碱溶液从阴极区导出,注意题中阳离子交换膜仅允许Na+通过的特点.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案【题目】某学生用0.100 0molL﹣1盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液.需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要 .
(2)滴定: Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上.
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“0”刻度线以下,并记录读数.
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液.
Ⅳ.用标准液滴定至终点,记录滴定管液面读数.
①上述滴定步骤中有错误的是(填编号) , 该错误操作会导致测定结果
(填“偏大”“偏小”或“无影响”).
②步骤Ⅳ中滴定时眼睛应 , 判断滴定终点的现象是 .
③若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果(填“偏大”“偏小”或“无影响”).
(3)按正确操作测得有关数据记录如下:
滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.20 | 20.38 |
第二次 | 20.00 | 4.00 | 24.20 |
第三次 | 20.00 | 2.38 | a |
①a的读数如图所示,则a=;
②烧碱样品的纯度为%.
【题目】某同学用中和滴定法测定某烧碱的纯度,实验过程如下:
(1)a.配制待测液:称取4.1g固体烧碱样品(杂质不与酸反应)配制成250mL溶液. b.滴定
①用量取10.00mL待测液.
②向锥形瓶中加入几滴酚酞,用0.201 0molL﹣1的标准盐酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,直到时停止滴定.
(2)数据处理
实验次 | 盐酸溶液体积 | 氢氧化钠溶液体积 |
1 | 19.90 | 10.00 |
2 | 20.10 | 10.00 |
3 | 22.00 | 10.00 |
4 | 20.00 | 10.00 |
根据上述表格,选取合适的数据,计算待测烧碱溶液的浓度为 , 烧碱的纯度为(保留两位小数).
(3)一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验室中配制盐酸标准溶液,然后用其滴定某未知浓度的NaOH溶液.下列有关说法中正确的是(多选)
A.实验中所用到的滴定管、容量瓶,在使用前均需要检漏
B.如果实验中需用80mL的稀盐酸标准溶液,配制时应选用100mL容量瓶
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀盐酸,则测得的NaOH溶液的浓度将偏大
E.配制溶液时,定容时俯视读数,则导致实验结果偏大
F.中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大
G.锥形瓶用蒸馏水洗浄后,有少量蒸馏水残留,则导致实验结果偏小
H.滴定前滴定管尖嘴有气泡,滴定后气泡消失,则导致实验结果偏大.