题目内容
【题目】浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4﹒7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
![]()
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是________。
(2)0.10mol·L-1莫尔盐溶液中离子浓度由大到小的顺序为_________;
(3)常温下,若0.1 mol﹒L-1 (NH4)2SO4溶液的pH=5,求算NH3﹒H2O的电离平衡常数Kb=___________
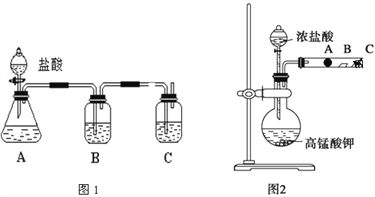
(4)为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为c mol﹒L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
实验次数. | 第一次 | 第二次 | 第三次 |
消耗高锰酸钾溶液体积/mL | .25.52, | 25.02 | 24.98 |
滴定过程中发生反应的离子方程式为:_______________。滴定终点的现象是____________________。
通过实验数据计算的该产品纯度为_________(用字母ac表)。上表中第一次实验中记录数据明显大于后两次,其原因可能是____________(填符号)。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
【答案】(l)防止Fe2+被氧化为Fe3+,(2分)
(2)c(SO42-)>c(NH4-)>c(Fe2+)>c(H+)>c(OH-)(2分)
(3)2×10-5(2分)
(4)MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;(2分)
滴入最后一滴高锰酸钾溶液,锥形瓶内溶液由浅绿色变为浅紫色,且30s不变色;(2分)
![]() ×100%(2分)BC(2分)
×100%(2分)BC(2分)
【解析】
试题分析:(1)Fe2+离子不稳定,易被氧气氧化为Fe3+离子,剩余少量铁粉防止Fe2+离子被氧化为Fe3+离子;
(2)Fe2+水解,NH4+水解,溶液呈酸性,两者的浓度降低,溶液中离子浓度由大到小的顺序为:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-);
(4)常温下,若0.10 molL-1(NH4)2SO4溶液的pH=5,溶液中c(H+)=10-5molL-1,故溶液中c(OH-)=10-9molL-1,根据电荷守恒有:c(NH4+)+c(H+)=c(OH-)+2c(SO42-),即c(NH4+)+10-5molL-1=10-9molL-1+0.20 molL-1,则c(NH4+)=(0.20+10-9-10-5)molL-1,根据物料守恒计算溶液中c(NH3H2O)=0.20molL-1-(0.20+10-9-10-5)molL-1=(10-5-10-9)molL-1,故NH4++H2O![]() NH3H2O+H+的平衡常数的表达式为
NH3H2O+H+的平衡常数的表达式为![]() =
= ![]() =5×10-10,氨水中存在下列的电离平衡:NH3H2O
=5×10-10,氨水中存在下列的电离平衡:NH3H2O![]() NH4++OH-,电离平衡常数为K,水的电离平衡可知:5×10-10×K=1×10-14,所以K=2×10-5;
NH4++OH-,电离平衡常数为K,水的电离平衡可知:5×10-10×K=1×10-14,所以K=2×10-5;
(4)利用高锰酸钾的强氧化性,Fe2+的强还原性,两者发生氧化还原反应,Fe2+被氧化成Fe3+↑1,Mn由+7价→+2↓5,最小公倍数5,根据原子个数、电荷守恒,即MnO4-+5Fe2++ 8H+=Mn2+ + 5Fe3++ 4H2O;向溶液中滴加中高锰酸钾,高锰酸钾显紫红色,因此滴定到终点:滴入最后一滴高锰酸钾溶液,锥形瓶内溶液由浅绿色变为浅紫色,且30s不变色;因为第一次与第二次、第三次相差较大,忽略不计,消耗高锰酸钾溶液的体积为(25.02+24.98)mL÷2=25mL,根据离子反应方程式,得出:n[((NH4)2SO4·FeSO4·6H2O]=5n(KMnO4)=25×10-3×c×5mol,则500mL溶液中含有n[(NH4)2SO4·FeSO4·6H2O]=25×10-3×c×5×500/25mol=2.5cmol,所以质量分数=2.5c×392/a×100%=980c/a×100%;A、俯视读数,造成所读的数偏小,A错误;B、滴定管尖嘴有气泡,滴定结束无气泡,所消耗的液体体积增加,B正确;C、锥形瓶用待测液润洗,待测液的物质的量增加,则消耗高锰酸钾的体积增加,C正确;D、三次使用的高锰酸钾都是一样的,消耗的高锰酸钾体积应是相同的,D错误,答案选BC。