题目内容
20.下列说法正确的是( )| A. | 其他条件不变时增大压强,能使全气体反应体系中活化分子百分数增加 | |
| B. | 中和反应都是放热反应 | |
| C. | 在FeCl3溶液和KSCN溶液反应的平衡体系中,加入KCl固体,平衡逆向移动 | |
| D. | 熵增大的反应不一定自发,但自发反应熵定增大 |
分析 A、增大气体反应体系的压强,活化分子百分数不变;
B、中和反应都是放热反应;
C、根据实际参加反应的离子浓度分析,加入少量KCl固体,溶液中Fe3+、SCN-浓度不变;
D、依据△H-T△S<0反应自发进行,△H-T△S>0属于非自发进行分析.
解答 解:A、增大气体反应体系的压强,体积减小,则反应物浓度增大,单位体积中活化分子数增多,但活化分子百分数不变,故A错误;
B、中和反应都是放热反应,故B正确;
C、根据实际参加反应的离子浓度分析,化学平衡为Fe3++3SCN-=Fe(SCN)3,加入少量KCl固体,溶液中Fe3+、SCN-浓度不变,溶液颜色不变,故C错误;
D、依据△H-T△S<0反应自发进行,△H-T△S>0属于非自发进行分析,熵增大反应△S>0,△H>0低温下反应自发进行,△S<0,△H<0,低温下反应自发进行,自发反应熵不一定增大,故D错误;
故选B.
点评 本题考查了压强对活化分子的影响,平衡移动以及反应自发进行的判断依据和分析方法,掌握基础是关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列说法中正确的是( )
| A. | 物质发生化学反应时都伴随着能量变化,伴随能量变化的变化一定是化学变化 | |
| B. | 需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 | |
| C. | 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 | |
| D. | 因为3O2═2O3是吸热反应,所以臭氧比氧气更稳定 |
15.已知镁粉与冷水几乎不反应,与热水反应缓慢.市场上购买的“即热饭盒”底部有两层,一层装水,另一层是镁粉与铁粉的混合物,当水与金属粉末接触时会发生反应Mg+2H2O═Mg(OH)2+H2↑.则下列说法不正确的是( )
| A. | “即热饭盒”的工作原理是将化学能转化为热能 | |
| B. | 上述反应中,反应物的总焓大于生成物的总焓 | |
| C. | 铁粉的作用是催化剂 | |
| D. | 上述反应的反应热Q为正值 |
5.在氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂.下列反应中属于氧化还反应且与Br2+SO2+2H2O═H2SO4+2HBr相比较,水的作用相同的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2F2+2H2O═4HF+O2 | D. | CaO+H2O═Ca(OH)2 |
9.12.8gCu和一定浓度的硝酸200mL充分反应,生成的NO2和NO标况下为11.2L,若反应后溶液中有0.3mol H+,则原硝酸溶液的物质的量浓度为( )
| A. | 4.5mol•L-1 | B. | 5mol•L-1 | C. | 6mol•L-1 | D. | 8mol•L-1 |
10.下列物质中不能用来区分乙酸、乙醇、苯、四氯化碳的是( )
| A. | 溴水 | B. | 酸性髙锰酸钾溶液 | ||
| C. | 碳酸钠溶液 | D. | 紫色石蕊溶液 |

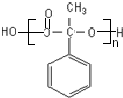 ;
;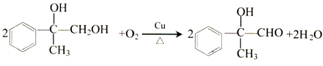 ,
,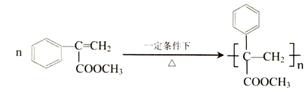 ;
;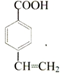 (写结构简式).
(写结构简式).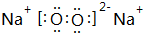 ,Z的化学式SiO2;
,Z的化学式SiO2; 已知:A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成食品包装材料.
已知:A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成食品包装材料.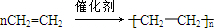 .
.