题目内容
3.下列物质长期放在空气中质量不增加的是( )| A. | 氢氧化钠固体 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 生石灰 |
分析 A、氢氧化钠固体在空气中易潮解并能与二氧化碳发生化学变化生成碳酸钠;
B、浓硫酸具有吸水性;
C、浓盐酸具有强烈的挥发性;
D、生石灰长期放在空气中生成碳酸钙.
解答 解:A、由于氢氧化钠固体在空气中易潮解并能与二氧化碳发生化学变化生成碳酸钠,从而使固体质量增加,故A错误;
B、由于浓硫酸具有吸水性,因此溶液的质量会增加,故B错误;
C、由于浓盐酸具有强烈的挥发性,从而溶液的质量减少,故C正确;
D、生石灰长期放在空气中生成碳酸钙,质量增加,故D错误;
故选:C.
点评 此题是一道物质变化的考查题,解题的关键是对选项中的物质在空气中的变化以及反应的实质的了解,属基础性知识考查题.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
11.有关化学反应方向的判断,下列说法中正确的是( )
| A. | 放热反应均是自发反应 | |
| B. | 物质的量增加的反应,△S为正值 | |
| C. | 如果△H和△S均为正值,当温度升高时,反应可能自发进行 | |
| D. | △S为正值的反应均是自发反应 |
15.下列元素中,最高正化合价最大的是( )
| A. | C | B. | F | C. | S | D. | Ne |
12.用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A. | CO2和O2组成的混合物中共有NA个分子,其中氧原子数为2NA | |
| B. | 78g过氧化钠与足量的CO2和H2O(g)混合气体充分反应,转移的电子数一定为NA | |
| C. | 1 mol 氢氧根和1 mol 羟基中含有的质子数均为 9 NA | |
| D. | 标准状况下,2.24L氯仿(CHCl3)中含有C-Cl数目为0.3NA |
13.下列叙述正确的是( )
| A. | 构成原电池正极和负极的材料必须是两种金属 | |
| B. | 由铜、锌作电极与硫酸铜溶液构成的原电池中铜作负极 | |
| C. | 电子由外导线从锌流向铜,进入硫酸溶液后被H+得到而释放出H2 | |
| D. | 铜锌原电池工作时,若电路中通过0.4 mole-,锌片质量将减少13g |
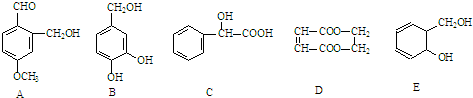
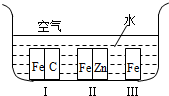 (1)反应A+3B?2C+2D在四种不同情况下的反应速率分别如下:
(1)反应A+3B?2C+2D在四种不同情况下的反应速率分别如下: