题目内容
20.下列事实可证明氨水是弱碱溶液的是( )| A. | 氨水能被弱酸醋酸中和 | |
| B. | 铵盐受热易分解 | |
| C. | 氨水可以使酚酞试液变红 | |
| D. | 0.lmol/L氨水溶液,常温时pH约为11 |
分析 只要证明一水合氨部分电离就能证明一水合氨是弱电解质,则氨水是弱碱,据此分析解答.
解答 解:A.氨水能被弱酸醋酸中和,说明氨水是碱,但没有明确一水合氨部分电离,所以不能证明氨水是弱碱,故A错误;
B.铵盐受热易分解说明铵盐不稳定,不能明确一水合氨部分电离,所以不能证明氨水是弱碱,故B错误;
C.氨水可以使酚酞试液变红色,说明氨水溶液呈碱性,但不能明确一水合氨部分电离,所以不能证明氨水是弱碱,故C错误;
D.0.lmol/L氨水溶液,常温时pH约为11,如果一水合氨完全电离,该氨水溶液pH应该是13,实际上约为11,说明一水合氨部分电离,为弱电解质,故D正确;
故选D.
点评 本题考查弱电解质的判断,为高频考点,明确强弱电解质根本区别是解本题关键,注意不能根据电解质溶解性大小、电解质溶液导电能力大小判断强弱电解质,要根据电离程度判断,为易错题.

练习册系列答案
相关题目
6.下列元素中,属于第ⅣA族的是( )
| A. | 钠 | B. | 镁 | C. | 碳 | D. | 氮 |
7.NA代表阿伏加德罗常数,则关于热化学方程C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1300kJ•mol-1的说法中,正确的是( )
| A. | 有10NA个电子转移时,放出1300kJ的能量 | |
| B. | 有44.8LCO2气体生成时,放出1300kJ的能量 | |
| C. | 有NA个水分子生成且为液体时,吸收1300kJ的能量 | |
| D. | 有4NA个碳氧共用电子对生成时,放出1300kJ的能量 |
5. 已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是( )
 已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是( )| A. | T1<T2 P1>P2 m+n<P Q<0 | B. | T1>T2 P1<P2 m+n>P Q>0 | ||
| C. | T1<T2 P1<P2 m+n<P Q>0 | D. | T1>T2 P1<P2 m+n>P Q<0 |
12.在100℃和200kPa的条件下,密闭容器中进行的化学反应aA(g)?bB(g)+cC(g)达到平衡状态,在维持体系温度不变的条件下逐步压缩体积,体系压强也逐渐增大,测定不同压强下反应再次建立平衡时物质B的浓度,结果如表所示.
根据表中的数据,回答下列问题(提示:温度和压强的改变可能会对物质的聚集状态产生影响)
(1)压强从200kPa增加到500kPa时,平衡不移动(填“正向”或“逆向”或“不”),理由是浓度增大的倍数和压强增大的倍数相同.
(2)压强从500kPa增加到1000kPa时,平衡正向移动(填“正向”或“逆向”或“不”),其原因可能为加压至1000kPa时,C物质变成了非气态物质.
(3)化学方程式中的化学计量数的关系是:a=b+c(填“?”“?”或“?”)
| 压强(kPa) | 200 | 500 | 1000 |
| B的浓度(mol/L) | 0.04 | 0.1 | 0.27 |
(1)压强从200kPa增加到500kPa时,平衡不移动(填“正向”或“逆向”或“不”),理由是浓度增大的倍数和压强增大的倍数相同.
(2)压强从500kPa增加到1000kPa时,平衡正向移动(填“正向”或“逆向”或“不”),其原因可能为加压至1000kPa时,C物质变成了非气态物质.
(3)化学方程式中的化学计量数的关系是:a=b+c(填“?”“?”或“?”)
10.在一个定容密闭容器中,加入2molA和1molB发生如下反应:2A(g)+B(g)?3C(g)+D(g),达到平衡时C的浓度为1.2mol/L.若维持温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2mol/L的是( )
| A. | 4molA+2molB | B. | 1.5molC+0.5molD | C. | 3molC+1molD | D. | 3molA+1molB |
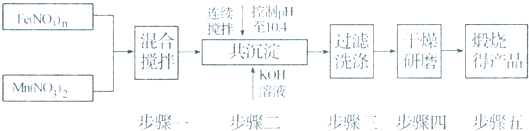
 2NH3.
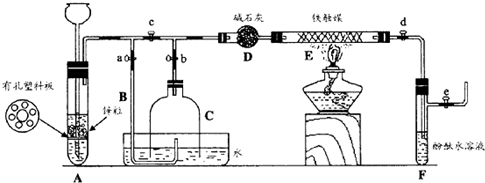
2NH3.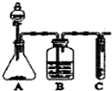 Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质
Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质