题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
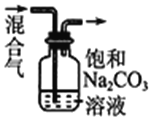
A.“84”消毒液中,SiO![]() 、CO
、CO![]() 、Na+、K+
、Na+、K+
B.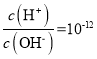 的溶液中NH
的溶液中NH![]() 、Ca2+、C1-、NO3-
、Ca2+、C1-、NO3-
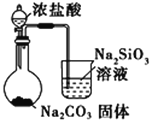
C.0.1mol/LNaA1O2溶液中:HCO![]() 、NH4+、SO
、NH4+、SO![]() 、Fe3+
、Fe3+
D.pH=1的溶液中:Na+、K+、Cl-、S2O![]()
【答案】A
【解析】
A.“84”消毒液主要成分是NaClO,SiO![]() 、CO
、CO![]() 、Na+、K+与NaClO均不发生反应,能大量共存,故A选;
、Na+、K+与NaClO均不发生反应,能大量共存,故A选;
B.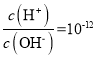 的溶液呈碱性,NH
的溶液呈碱性,NH![]() 与OH-反应生成NH3·H2O,不能大量存在,故B不选;
与OH-反应生成NH3·H2O,不能大量存在,故B不选;
C.0.1mol/LNaA1O2溶液中,偏铝酸根与HCO![]() 、NH4+、Fe3+均反应,碳酸氢根与铁离子反应,不能大量共存,故C不选;
、NH4+、Fe3+均反应,碳酸氢根与铁离子反应,不能大量共存,故C不选;
D.pH=1的溶液呈酸性,发生反应2H++S2O![]() =S↓+SO2↑+H2O,不能大量共存,故D不选;
=S↓+SO2↑+H2O,不能大量共存,故D不选;
故选A。

【题目】甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇时,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1= -99kJmol-1
CH3OH(g) △H1= -99kJmol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2= 58kJmol-1
CH3OH(g)+H2O(g) △H2= 58kJmol-1
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3=+41kJmol-1
CO(g)+H2O(g) △H3=+41kJmol-1
(1)一定温度下,向体积为2L的密闭容器中加入CO和H2,假设只发生反应①,达平衡后测得各组分浓度如下:
物质 | CO | H2 | CH3OH |
浓度(molL-1) | 0.9 | 1.0 | 0.6 |
①列式并计算平衡常数K=___。
②若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是___。
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正__v逆(填“>”、“<”或“=”)。
(2)在实际生产中,当合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图所示。
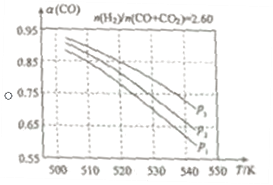
α(CO)值随温度升高而___(填“增大”或“减小”),其原因是___。图中的压强由大到小为___,其判断理由是___。