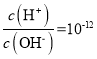题目内容
【题目】下列有关化学反应原理的应用叙述中,正确的是![]()
A.用明矾净水是因为![]() 水解生成的
水解生成的![]() 胶粒具有较强的吸附性
胶粒具有较强的吸附性
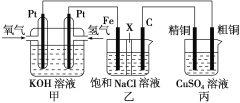
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀
D.为了防止钢铁锈蚀,把输油管的铸铁管连接外加直流电源的正极
【答案】A
【解析】
![]() 水解生成具有吸附性的
水解生成具有吸附性的![]() 胶粒,可除去水中的悬浮物,从而达到净水的目的,故A正确;
胶粒,可除去水中的悬浮物,从而达到净水的目的,故A正确;
B.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,![]() 溶液做电解液,阳极上铜失电子发生氧化反应,阴极上铜离子得电子发生还原反应,故B错误;
溶液做电解液,阳极上铜失电子发生氧化反应,阴极上铜离子得电子发生还原反应,故B错误;
C.不锈钢和铝合金等耐腐蚀,所以合金也可能耐腐蚀,故C错误;
D.铸铁连接直流电源正极时作电解池阳极,加速被腐蚀,故D错误;
答案:A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】常温,下列实验操作及现象与推论不相符的是( )
选项 | 操作及现象 | 推论 |
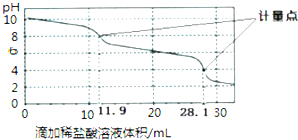
A | 用pH试纸测得0.1mol/LCH3COOH溶液pH约为3 | CH3COOH是弱电解质 |
B | 向某无色溶液中加入足量稀盐酸,产生无色无味气体;再将该气体通入澄清石灰水,产生白色浑浊 | 溶液中可能含有CO |
C | 用pH计测定相同浓度的CH3COONa溶液和NaClO溶液的pH,前者的pH小于后者的 | HClO的酸性弱于CH3COOH |
D | 向2mL1mol/LNaOH溶液中加入1mL0.1mol/LMgCl2溶液,产生白色沉淀;再加入1mL0.1mol/LFeCl3溶液,产生红褐色沉淀 | Mg(OH)2沉淀转化为Fe(OH)3沉淀 |
A.AB.BC.CD.D