题目内容
6.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的某性质)把与下面元素有关性质相符的曲线标号填入相应括号中:
(1)ⅡA族元素的最外层电子数b
(2)第三周期元素的最高化合价c
(3)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径d
(4)第三周期元素随原子序数递增原子半径的变化(不包括惰性气体)a
(5)碱金属的阳离子氧化能力(不包括钫)a.
分析 (1)ⅡA族元素的价电子数为2,随核电荷数增大,价电子数不变;
(2)第三周期元素的最高化合价,随核电荷数增大,最高化合价由+1价递增到+7,最后以稀有气体0价结束;
(3)电子层结构相同,核电荷数越大,离子半径越小,最外层电子数相同,电子层越多,离子半径越大;
(4)同周期随原子序数增大,原子半径减小;
(5)碱金属随核电荷数增大,金属性增强,阳离子氧化性减弱.
解答 解:(1)ⅡA族元素的价电子数为2,随核电荷数增大,价电子数不变,故图b符合,故选:b;
(2)第三周期元素的最高化合价,随核电荷数增大,最高化合价由+1价递增到+7,最后以稀有气体0价结束,故图c符合,故选:c;
(3)电子层结构相同,核电荷数越大,离子半径越小,所以离子半径Na+>Mg2+>Al3+、P3->S2->Cl-,最外层电子数相同,电子层越多,离子半径越大,所以离子半径Cl->Na+.所以离子半径P3->S2->Cl->Na+>Mg2+>Al3+,故图d符合,故选:d;
(4)同周期主族元素,随原子序数递增原子半径减小,故图a符合,故选:a;
(5)碱金属随核电荷数增大,金属性增强,阳离子氧化性减弱,故图a符合,故选:a.
点评 本题以图象形式考查元素周期律,难度不大,注意规律的归纳与总结与理解,有利于基础知识的巩固.

练习册系列答案
相关题目
17.接触法生产硫酸的过程中,对废气、废水、废渣、废热的处理正确的是( )
①尾气用氨水处理
②污水用石灰乳处理
③废渣用来造水泥、炼铁
④设置废热锅炉产生蒸汽、供热或发电.
①尾气用氨水处理
②污水用石灰乳处理
③废渣用来造水泥、炼铁
④设置废热锅炉产生蒸汽、供热或发电.
| A. | ①②③④ | B. | ①③④ | C. | ①②③ | D. | ①② |
14. A,B,C,D,E,F是原子序数依次增大的前四周期的常见元素,其相关信息如下表:
A,B,C,D,E,F是原子序数依次增大的前四周期的常见元素,其相关信息如下表:
回答下列问题:
(1)基态E原子的核外M层电子云有9种不同的伸展方向,基态E原子核外价电子排布式为3d54s1,元素F属于d区.
(2)A与C形成的最简单分子的空间构型为三角锥形,中心原子的杂化方式为sp3.
(3)B,C,D第一电离能由大到小的顺序是N>O>C(用元素符号表示);由B,C,D中的两种元素组成的常见分子互为等电子体的是N2O和CO2
(4)E元素可以形成配位 数为6的两种配合物,它们的化学式都是ECl3﹒6H2O,其中一种呈亮棕色,与硝酸银溶液反应时,能沉淀出$\frac{1}{3}$的氯元素,该配合物可表示为[Cr(H2O)4Cl2]Cl•2H2O.
(5)元素F的一种氯化物的晶胞结构如图 所示(黑球表示F原子,白球表示氯原子),每个氯原子周围与之距离最近的氯原子个数为12;若晶胞的密度为4.14g﹒cm-3,该晶胞的边长为$\root{3}{\frac{398}{4.14{N}_{A}}}$cm(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)
 A,B,C,D,E,F是原子序数依次增大的前四周期的常见元素,其相关信息如下表:
A,B,C,D,E,F是原子序数依次增大的前四周期的常见元素,其相关信息如下表:| A | 宇宙中含量最丰富的元素 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | 最高价氧化物对应的水化物与其氢化物反应生成盐 |
| D | 原子核外电子有8种不同的运动状态 |
| E | 基态原子核外有六个未成对电子 |
| F | 原子最外层只有一个电子 |
(1)基态E原子的核外M层电子云有9种不同的伸展方向,基态E原子核外价电子排布式为3d54s1,元素F属于d区.
(2)A与C形成的最简单分子的空间构型为三角锥形,中心原子的杂化方式为sp3.
(3)B,C,D第一电离能由大到小的顺序是N>O>C(用元素符号表示);由B,C,D中的两种元素组成的常见分子互为等电子体的是N2O和CO2
(4)E元素可以形成配位 数为6的两种配合物,它们的化学式都是ECl3﹒6H2O,其中一种呈亮棕色,与硝酸银溶液反应时,能沉淀出$\frac{1}{3}$的氯元素,该配合物可表示为[Cr(H2O)4Cl2]Cl•2H2O.
(5)元素F的一种氯化物的晶胞结构如图 所示(黑球表示F原子,白球表示氯原子),每个氯原子周围与之距离最近的氯原子个数为12;若晶胞的密度为4.14g﹒cm-3,该晶胞的边长为$\root{3}{\frac{398}{4.14{N}_{A}}}$cm(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)
1.下列说法正确的是( )
| A. | 3p2表示3p能级有两个轨道 | |
| B. | 处于最低能量的原子叫做基态原子 | |
| C. | 同一原子中,1s、2s、3s电子的能量逐渐减小 | |
| D. | 同一原子中,1p、2p、3p电级的轨道数依次增多 |
11.常温下,已知有某浓度的CH3COOH溶液,下列说法不正确的是( )
| A. | 该溶液与等浓度NaOH溶液等体积混合后,pH>7 | |
| B. | 测得Na2CO3的碱性比CH3COONa溶液强,因此得出醋酸的酸性比碳酸强的结论 | |
| C. | 若向该溶液中加入少量CH3COONa固体,恢复至常温后,c(CH3COOH)比原来增大 | |
| D. | 若向一定浓度的CH3COONa溶液中加入少量CH3COONa固体,恢复至常温后,其水解程度比原来下降 |
18.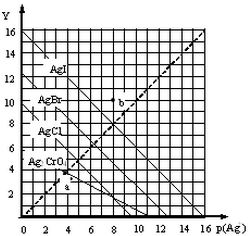 卤化银AgX及Ag2CrO4的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)═-lgc(Ag+),纵坐标Y=-lgc(X-)或lgc(CrO42-).下列说法正确的是( )
卤化银AgX及Ag2CrO4的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)═-lgc(Ag+),纵坐标Y=-lgc(X-)或lgc(CrO42-).下列说法正确的是( )
 卤化银AgX及Ag2CrO4的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)═-lgc(Ag+),纵坐标Y=-lgc(X-)或lgc(CrO42-).下列说法正确的是( )
卤化银AgX及Ag2CrO4的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)═-lgc(Ag+),纵坐标Y=-lgc(X-)或lgc(CrO42-).下列说法正确的是( )| A. | 该温度下Ag2CrO4的Ksp约为1×10-22 | |
| B. | a点可表示AgCl的饱和溶液 | |
| C. | b点c(Ag+)=c(I-) | |
| D. | 该温度下AgCl、AgBr饱和溶液中:c(Cl-)<c(Br-) |
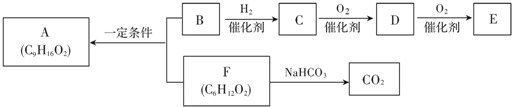
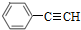 的合成方法有:
的合成方法有: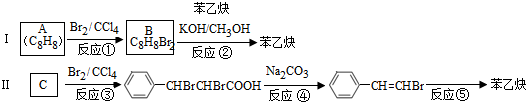

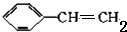 ,反应①,②涉及的反应类型是加成反应、消去反应.
,反应①,②涉及的反应类型是加成反应、消去反应.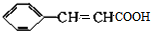 ,反应⑤的化学方程式为
,反应⑤的化学方程式为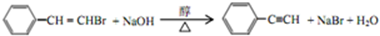 (注明反应条件)
(注明反应条件)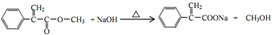 .
.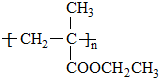 单体的结构简式为CH2=C(CH3)COOCH2CH3.用类似反应⑥的方法,利用合适的原料可以合成该单体,化学方程式为
单体的结构简式为CH2=C(CH3)COOCH2CH3.用类似反应⑥的方法,利用合适的原料可以合成该单体,化学方程式为 .
.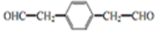 .
.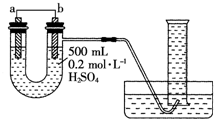 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题: