题目内容
13.已知某化合物由K、Fe、O三种元素组成,且钾与氧两种元素的物质的量之比为1:2,则该化合物的化学式为KFeO2或K2FeO4.分析 在化合物中K元素呈现+1价,O元素一般呈现-2价,若钾与氧两种元素的物质的量之比为1:2,那么可以设K的个数为n,据此计算即可.
解答 解:在化合物中K元素呈现+1价,O元素一般呈现-2价,若钾与氧两种元素的物质的量之比为1:2,那么可以设K的个数为n,那么O的个数为2n,即铁元素化合价=2n×2-n=3n,n=1,那么Fe的化合价为+3价,此物质为:KFeO2,若n=2,则Fe的化合价为+6价,产物为:K2FeO4,故答案为:KFeO2或K2FeO4.
点评 本题主要考查的是化学式的确定,掌握化合物中元素化合价代数和为0是解决本题的关键,有一定难度.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
3.下列电离方程式中,正确的是( )
| A. | NaHCO3═Na++H++CO32- | B. | Ba(OH)2═Ba2++OH- | ||
| C. | Al2(SO4)3═2Al3++3SO42- | D. | NH3•H2O═NH4++OH- |
1.含硅元素的物质有很多用途,下列说法不正确的是( )
| A. | 水玻璃是硅酸钠的水溶液,可用作木材防火剂的原料 | |
| B. | 化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是SiO2 | |
| C. | 我国的三峡大坝使用了大量水泥,水泥是硅酸盐材料 | |
| D. | 光导纤维主要成份为SiO2,可用作太阳能电池 |
8.下列实验操作中,正确的是( )
| A. | 用酒精萃取碘水中的碘 | |
| B. | 蒸馏时,冷却水从冷凝管的上口通入,下口流出 | |
| C. | 用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出 | |
| D. | 配制1.00 mol/L NaCl溶液时,将称好的NaCl固体直接放入容量瓶中溶解 |
5.下列依据相关实验得出的结论正确的是( )
| A. | 向FeCl2溶液中滴加少量KSCN溶液变血红色,说明FeCl2完全被氧化成FeCl3 | |
| B. | 相同条件下,Na2CO3溶液的碱性强于C6H5ONa,说明C6H5OH的酸性强于H2CO3 | |
| C. | 向漂白粉上加入较浓的盐酸,产生的气体不能使湿润淀粉碘化钾试纸变蓝,说明该漂白粉已经失效 | |
| D. | 向浓度均为0.1 mol•L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液,产生黄色沉淀,说明Ksp(AgCl)<Ksp(AgI) |
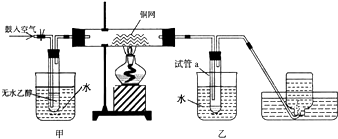

 ;
; ;
; (填结构简式).
(填结构简式).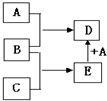 已知A、B、C均为常见单质,其中A是金属,B、C是非金属,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).
已知A、B、C均为常见单质,其中A是金属,B、C是非金属,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).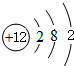 ,A和E在一定条件下反应生成D的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO.
,A和E在一定条件下反应生成D的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO.