题目内容
【题目】根据要求完成下列化学方程式或离子方程式。
(1)利用铝热反应焊接钢轨的化学方程式为_________________________。
(2)工业制备粗硅的化学方程式_________________。
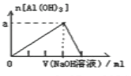
(3)氯化铝溶液与氨水制备氢氧化铝的离子方程式为_________________。
(4)用离子反应方程式说明为何装氢氧化钠溶液不能用玻璃塞_________________。
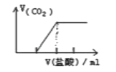
(5)用盐酸除去铜锈(碱式碳酸铜)的离子反应_________________。
【答案】2Al + Fe2O3![]() 2Fe + Al2O3 2C+SiO2
2Fe + Al2O3 2C+SiO2![]() Si+2CO Al3++3NH3·H2O=Al(OH)3↓+ 3NH4+ SiO2 + 2OH- = SiO32- + H2O Cu2(OH)2CO3+ 4H+= 2Cu2++ 3H2O+ CO2↑
Si+2CO Al3++3NH3·H2O=Al(OH)3↓+ 3NH4+ SiO2 + 2OH- = SiO32- + H2O Cu2(OH)2CO3+ 4H+= 2Cu2++ 3H2O+ CO2↑
【解析】
(1)用铝热反应焊接钢轨是利用铝能够还原氧化铁生成铁;
(2)工业上制备粗硅,是利用碳在高温下还原二氧化硅;
(3)氯化铝溶液与氨水反应生成氢氧化铝和氯化铵;
(4)氢氧化钠能够与玻璃中的二氧化硅反应生成硅酸钠,长时间后,瓶塞不容易打开;
(5)盐酸与碱式碳酸铜反应生成氯化铜、水和二氧化碳;
据此分析书写方程式。
(1)用铝热反应焊接钢轨是利用铝能够还原氧化铁,反应的化学方程式为2Al + Fe2O3![]() 2Fe + Al2O3,故答案为:2Al + Fe2O3
2Fe + Al2O3,故答案为:2Al + Fe2O3![]() 2Fe + Al2O3;
2Fe + Al2O3;
(2)工业上利用碳在高温下还原二氧化硅制备粗硅,反应的化学方程式为2C+SiO2![]() Si+2CO,故答案为:2C+SiO2
Si+2CO,故答案为:2C+SiO2![]() Si+2CO;
Si+2CO;
(3)氯化铝溶液与氨水制备氢氧化铝的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+ 3NH4+,故答案为:Al3++3NH3·H2O=Al(OH)3↓+ 3NH4+;
(4)氢氧化钠能够与玻璃中的二氧化硅反应生成硅酸钠,长时间后,瓶塞不容易打开,因此盛装氢氧化钠溶液的试剂瓶不能用玻璃塞,反应的离子方程式为SiO2 + 2OH -= SiO32- + H2O,故答案为:SiO2 + 2OH -= SiO32- + H2O;
(5)盐酸与碱式碳酸铜反应的离子方程式为Cu2(OH)2CO3+ 4H+= 2Cu2++ 3H2O+ CO2↑,故答案为:Cu2(OH)2CO3+ 4H+= 2Cu2++ 3H2O+ CO2↑。

 阅读快车系列答案
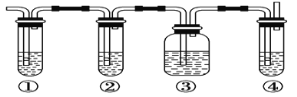
阅读快车系列答案【题目】(1)世界水产养殖协会介绍了一种利用电化学原理净化鱼池中水质的方法,其装置如图所示。请写出阴极的电极反应式 _________________________。
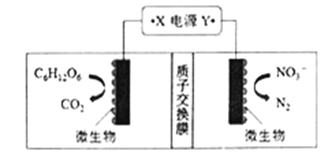
(2)甲醇可利用水煤气合成:CO(g)+2H2(g) ![]() CH3OH(g) △H<0. 一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变温度或压强时,平衡后CH3OH的体积分数 φCH3OH)变化趋势如图所示。下列说法正确的是___________。
CH3OH(g) △H<0. 一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变温度或压强时,平衡后CH3OH的体积分数 φCH3OH)变化趋势如图所示。下列说法正确的是___________。
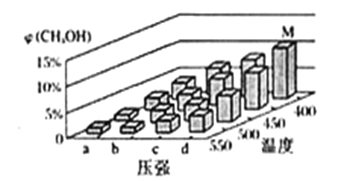
A.状态M,平衡时的CO转化率为10%
B.图中压强的大小关系是a<b<c<d
C.恒温恒压时,在原平衡体系中再充入适量甲醇,重新平衡后体系中甲醇的体积分数不变
D.当体系中 n(CO)/n(H2)的值不随时间变化时,体系达到平衡
(3)二氧化硫和碘水会发生如下二步反应:
反应 | 活化能 | |
第一步 | SO2+I2+2H2O | 9.2kJ·mo1-1 |
第二步 | I2+ I— | 23.5kJ·mo1-1 |
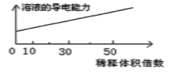
一定条件下,1mol SO2分别加入到体积相同、浓度不同的碘水中,体系达到平衡后,H+、I3—、SO42—的物质的量随n(I2)/n(SO2)的变化曲线如图 (忽略反应前后的体积变化)。

①有人认为X点的I—浓度小于Y点,你认为该观点是否正确________,原因是_________________。
②当n(I2)/n(SO2)=4时,请在下图画出体系中n (I—)反应时间的变化曲线。________
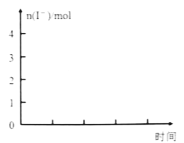
③化学兴趣小组拟采用下述方法来测定I2+I—![]() I3—的平衡常数(室温条件下进行,实验中溶液体积变化忽略不计):
I3—的平衡常数(室温条件下进行,实验中溶液体积变化忽略不计):
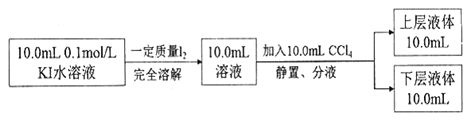
已知:I—和I3 —不溶于CCl4;:一定温度下,碘单质在四氯化碳和水混合液体中,碘单质的浓度比值 ![]() 即是一个常数(用Kd表示,称为分配系数),室温条件下 Kd=85。实验测得上层溶液中c(I3 —)=0.049mol/L,下层液体中c(I2)=0.085mol·L-1。结合上述数据,计算室温条件下I2+ I—
即是一个常数(用Kd表示,称为分配系数),室温条件下 Kd=85。实验测得上层溶液中c(I3 —)=0.049mol/L,下层液体中c(I2)=0.085mol·L-1。结合上述数据,计算室温条件下I2+ I—![]() I3—的平衡常数K=_______(保留三位有效数字)。
I3—的平衡常数K=_______(保留三位有效数字)。