题目内容
【题目】下列有机化合物对应类别的同分异构体数目最少的是(不考虑立体异构)
选项 | A | B | C | D |
分子式 | C9H12 | C5H12O | C4H8O2 | C4H8FCl |
类别 | 芳香烃 | 醇 | 酯 | 卤代烃 |
A.AB.BC.CD.D
【答案】C
【解析】
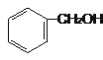
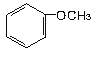
A.某有机物的分子式为C9H12,其同分异构体属于芳香烃,分子组成符合CnH2n﹣6,是苯的同系物,可以有一个侧链为:正丙基或异丙基,可以有2个侧链为:乙基、甲基,有邻、间、对3种,可以有3个甲基,有相邻、相偏、相均3种,共有8种;
B.戊烷的同分异构体有:CH3﹣CH2﹣CH2﹣CH2﹣CH3、![]() 、
、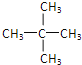 ,主链五个碳的有3种:CH2(OH)CH2CH2CH2CH3、CH3CH(OH)CH2CH2CH3、CH3CH2CH(OH)CH2CH3;主链四个碳的有4种:CH2(OH)CH(CH3)CH2CH3、CH3C(OH)(CH3)CH2CH3、CH3CH(CH3)CH(OH)CH3、CH3CH(CH3)CH2CH2(OH);主链三个碳的有1种:C(CH3)3CH2OH,共8种;
,主链五个碳的有3种:CH2(OH)CH2CH2CH2CH3、CH3CH(OH)CH2CH2CH3、CH3CH2CH(OH)CH2CH3;主链四个碳的有4种:CH2(OH)CH(CH3)CH2CH3、CH3C(OH)(CH3)CH2CH3、CH3CH(CH3)CH(OH)CH3、CH3CH(CH3)CH2CH2(OH);主链三个碳的有1种:C(CH3)3CH2OH,共8种;
C.C4H8O2属于酯类的同分异构体,为饱和一元酯。若为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇可以可知1个﹣OH取代丙烷中的H原子,丙烷分子中有2种H原子,形成的丙醇有2种,形成的酯有2种;若为乙酸与乙醇形成的酯,只有乙酸乙酯1种;若为丙酸与甲醇形成的酯,注意丙酸甲酯1种,故C4H8O2属于酯类的同分异构体共有4种;
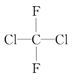
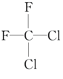
D.C4H8FCl,可看作Cl原子取代C4H9F的H原子,C4H9F有CH3CH2CH2CH2F、CH3CH2CH(CH3)F、(CH3)2CHCH2F、C(CH3)3F等4种,分别含有4、4、3、1种H,则共有12种;
则同分异构体数目最少的为C,故答案为C。

 阅读快车系列答案
阅读快车系列答案【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注。已知N2O5能与水发生反应,并放出大量的热。
Ⅰ.一定温度下,在恒容密闭容器中N2O5发生下列反应:2N2O5(g)![]() 4NO2(g)+O2(g)ΔH。
4NO2(g)+O2(g)ΔH。
(1)下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
则500s内NO2的生成速率为______________。
(2)反应达到平衡后,若再通入一定量N2O5,达到新平衡时,N2O5的转化率将______(填“增大”、“减小”、“不变”)。
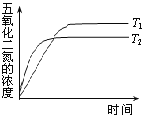
(3)在温度T1和T2时,N2O5的浓度与反应时间的关系如图所示。据此判断:T1______T2(填“>”、“<”或“=”,下同),ΔH______0。
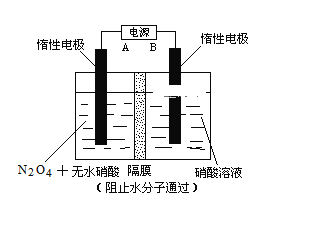
Ⅱ.下图所示装置,可用于制备N2O5气体。A是电源的____________(填“负极”或“正极”),电解池的阳极反应式为______________________________________________________。
【题目】NF3(三氟化氮)在常温常压下是无色、无味的气体,是微电子工业中一种优良的等离子蚀刻气体。回答下列问题:
(1)NF3的电子式为______,N元素的化合价为______。
(2)F2与NH3直接反应生成NF3的化学方程式为______。
(3)实验室模拟工业上利用电解熔融NH4HF2(NH4FHF)法制取NF3,阳极为以Ni为基本材料的合金(内含其他金属,忽略镍及其他金属的反应),阴极为碳素钢,电解废液可回收再利用。
①电解时NF3在______极生成;阴极产生的气体是______(填化学式)。
②电解后废液(含Ni少量Fe和Cu的单质及NH4HF2等)可经如下流程进行回收再利用:
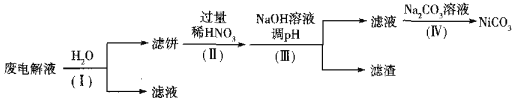
已知该实验条件下,部分金属离子开始沉淀与沉淀完全的pH如下表
金属离子 | Ni2+ | Fe2+ | Cu2+ | Fe3+ |
开始沉淀时的pH | 7.2 | 7.0 | 4.7 | 1.9 |
沉淀完全时的pH | 9.2 | 9.0 | 6.7 | 3.2 |
步骤I的目的是______;步骤Ⅱ滤饼中Ni溶于硝酸的离子方程式为______(HNO3的还原产物为NO);步骤Ⅲ调节pH时,理论上pH应控制的范围是______。