题目内容
【题目】C60是单纯由碳原子结合形成的稳定分子,结构如图。下列说法不正确的是
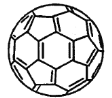
A.C60晶体易溶于苯、CS2,C60是非极性分子
B.1 mol C60分子中,含有δ键数目为60NA
C.C60与F2在一定条件下,发生反应生成C60F60
D.C60、金刚石和石墨是同素异形体
【答案】B
【解析】
C60是分子晶体,易溶于苯、CS2,根据相似相溶原理可知C60是非极性分子;根据结构可知,每一个碳原子形成3个δ键,但每个δ键被两个六边形共用,所以每个碳原子形成δ键的个数:![]() ,1 mol C60分子中有60个碳原子;同素异形体,是同种元素组成的不同形态的单质。
,1 mol C60分子中有60个碳原子;同素异形体,是同种元素组成的不同形态的单质。
A.C60是分子晶体,易溶于苯、CS2,根据相似相溶原理可知C60是非极性分子,故A正确;
B.根据结构可知,每一个碳原子形成3个δ键,但每个δ键被两个六边形共用,所以每个碳原子形成δ键的个数:![]() ,1 mol C60分子中有60个碳原子,δ键数目为:
,1 mol C60分子中有60个碳原子,δ键数目为:![]() ,故B错误;
,故B错误;
C.根据元素周期律,F的非金属性强于C,则F的氧化性强于C,可发生如下氧化还原反应反应:![]() ,故C正确;
,故C正确;
D.同素异形体,是同种元素组成的不同形态的单质,C60、金刚石和石墨是同素异形体,D正确;
答案选B。

练习册系列答案
相关题目