题目内容
下表给出几种氯化物的熔沸点:
对此有下列说法与表中数据一致的说法正确的是:( )
A.CaCl2晶体中的离子键比MgCl2晶体中的离子键弱; B.SiCl4是分子晶体;
C.801℃时,NaCl可形成气态; D.MgCl2水溶液不能导电。
| | NaCl | MgCl2 | CaCl2 | SiCl4 |
| 熔点(℃) | 801 | 712 | 782 | -68 |
| 沸点(℃) | 1465 | 1418 | 1600 | 57 |
A.CaCl2晶体中的离子键比MgCl2晶体中的离子键弱; B.SiCl4是分子晶体;
C.801℃时,NaCl可形成气态; D.MgCl2水溶液不能导电。
B
根据数据可知氯化钙的熔沸点高于氯化镁的熔沸点,因此CaCl2晶体中的离子键比MgCl2晶体中的离子键要强,A不正确。SiCl4的熔沸点很低,应该是分子晶体,B正确。氯化钠的熔点是801℃,沸点是1465℃,C是错误的。氯化镁是离子化合物,在溶液中能电离出离子,可以导电,D错误。所以答案选B。

练习册系列答案
相关题目
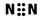

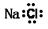
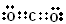
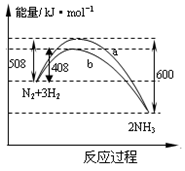
 NH3(g) △H= -92kJ·mol-1
NH3(g) △H= -92kJ·mol-1