题目内容
工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但钾却不能用电解熔融KCl的方法制得,因金属钾易溶于熔融态的KCl中而有危险,难获得钾,且降低电流效率。现生产钾是用属钠和熔化的KCl在一定的条件下反应制取:
 KCl + Na NaCl + K + Q (Q<0)
KCl + Na NaCl + K + Q (Q<0)
有关数据如下表:
(1) 工业上制取金属钾的化学原理是 ,在常压下金属钾转为气态从反应混合物中分离的最低温度约为 ,而反应的最高温度应低于 。
(2)在制取金属钾的过程中,为了提高原料的转化率可采取的措施是 。
(3)生产中常向反应物中通入一种气体,并将从反应器中导出的气体进行冷却得到金属钾,
且将该气体可循环利用,该气体是________。
a.干燥的空气 b.氮气 c.二氧化碳 d.稀有气体
(4)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为K= 。
 KCl + Na NaCl + K + Q (Q<0)
KCl + Na NaCl + K + Q (Q<0)有关数据如下表:
| | 熔点℃ | 沸点℃ | 密度(g/cm3) |
| Na | 97.8 | 882.9 | 0.97 |
| K | 63.7 | 774 | 0.86 |
| NaCl | 801 | 1413 | 2.165 |
| KCl | 770 | 1500(升华) | 1.984 |
(2)在制取金属钾的过程中,为了提高原料的转化率可采取的措施是 。
(3)生产中常向反应物中通入一种气体,并将从反应器中导出的气体进行冷却得到金属钾,
且将该气体可循环利用,该气体是________。
a.干燥的空气 b.氮气 c.二氧化碳 d.稀有气体
(4)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为K= 。
(1) 化学平衡移动原理(勒夏特列原理/钾蒸汽逸出使生成物浓度减小,平衡向正反应方向移动,可不断得到金属钾) 774℃ 882.9℃ (每空1分,共3分)
(2) 适当的升高温度、降低压强或移去钾蒸气 (2分)
(3)d (1分)
(4) c(K)/c(Na) (1分)
(2) 适当的升高温度、降低压强或移去钾蒸气 (2分)
(3)d (1分)
(4) c(K)/c(Na) (1分)
略

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
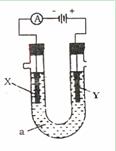
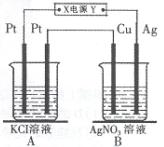
 阴极:2H3O++2e-→H2↑+2H2O
阴极:2H3O++2e-→H2↑+2H2O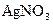 溶液中,通电电解,当电解液的pH从6.0变为3.0时(电解质溶液电解前后体积的变化忽略不计),则电极上应析出的银的质量是
溶液中,通电电解,当电解液的pH从6.0变为3.0时(电解质溶液电解前后体积的变化忽略不计),则电极上应析出的银的质量是