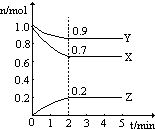��Ŀ����
����Ŀ����A��B��C��D���ֶ����ڵķǽ���Ԫ��(�䵥��Ҳ�ɷֱ���A��B��C��D��ʾ)������Ԫ�ص�ԭ��������B��D��C��A˳������D��CԪ�������ڱ���λ�����ڡ���һ�������£�B���Էֱ��A��C��D�������ɼס��ҡ��������C��D���Ͽɵö�����֪�ҡ������������и�����10�����ӣ����Ҽס��ҡ����������������µı仯��ϵ��
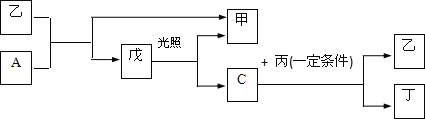
��ش��������⣺
��1����Ũ��Һ��һ�ֺ�ɫ��ĩ���ȿɵ�A��ʵ�����Ʊ�A�����ӷ���ʽΪ��__________________��
��2��BԪ�������ڱ��е�λ����______________��B��A��ȼ�յ�������____________��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
��C +����_____________________________________________��
�ڱ�+����D + �ң�___________________________________________��
��A +����D + �ף�_____________________________________________��
���𰸡� MnO2��4H++2Cl��![]() Mn2����Cl2����2H2O ��һ���ڵڢ�A�� ����ȼ�գ�������ɫ���� 4NH3��5O2
Mn2����Cl2����2H2O ��һ���ڵڢ�A�� ����ȼ�գ�������ɫ���� 4NH3��5O2![]() 4NO��6H2O 4NH3+6NO
4NO��6H2O 4NH3+6NO![]() 5N2+6H2O 2NH3+3Cl2��6HCl+N2
5N2+6H2O 2NH3+3Cl2��6HCl+N2
����������Ũ��Һ��һ�ֺ�ɫ��ĩ���ȿɵ�A�������Ȼ��⣬A�������������Ǵ����ᣬ��������ˮ��C������������ΪC��D�������ɶ���D��CԪ�������ڱ���λ�����ڣ���D��ԭ������С��O�ģ�DΪ��Ԫ��������NO����˱��ǰ�����B���Էֱ��A��C��D�������ɼס��ҡ�����������ҡ������������и�����10�����ӣ���BΪ��Ԫ�ء�
��1������������Ũ������ȷ�Ӧ�����Ȼ��̡�������ˮ�����ӷ���ʽΪ��MnO2��4H++2Cl��![]() Mn2����Cl2����2H2O����ȷ�𰸣�MnO2��4H++2Cl��
Mn2����Cl2����2H2O����ȷ�𰸣�MnO2��4H++2Cl��![]() Mn2����Cl2����2H2O��
Mn2����Cl2����2H2O��
��2��BԪ��Ϊ�⣬�����ڱ��е�λ���ǵ�һ���ڵڢ�A�壬�����������а���ȼ�գ�������ɫ���棻��ȷ�𰸣���һ���ڵڢ�A�壻����ȼ�գ�������ɫ���档
��3���ٰ�����������һ�������·�Ӧ����һ��������ˮ����ѧ����ʽ�� 4NH3��5O2![]() 4NO��6H2O ����ȷ����4NH3��5O2
4NO��6H2O ����ȷ����4NH3��5O2![]() 4NO��6H2O ��
4NO��6H2O ��
�ڰ�����һ��������һ�������·�����Ԫ�صĹ��з�Ӧ���ɵ�������ѧ����ʽ��4NH3+6NO![]() 5N2+6H2O ����ȷ����4NH3+6NO
5N2+6H2O ����ȷ����4NH3+6NO![]() 5N2+6H2O��
5N2+6H2O��
�������Ͱ�����Ӧ�����Ȼ���͵�������ѧ����ʽ��2NH3+3Cl2��6HCl+N2����ȷ�𰸣�2NH3+3Cl2��6HCl+N2��

 �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�