题目内容
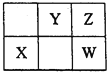
【题目】W、X、Y、Z四种短周期元素,在元素周期表中的位置如图所示,其中W元素的原子序数为Z元素原子序数的两倍,则下列说法正确的是
A. X位于元素周期表中的第3周期第ⅥA族
B. X、Y、Z三种元素对应原子的半径依次减小
C. XZ2和YZ2的结构和化学性质相似
D. 利用Y的含氧酸酸性强于W的含氧酸酸性,可证明非金属性W强于Y
【答案】B
【解析】
由于该四种元素均是短周期元素,W元素的原子序数为Z元素原子序数的两倍,且W与Z同主族,原子序数相差8,故Z为O,W为S,则X为Si,Y为N,据以上分析解答。
由于该四种元素均是短周期元素,W元素的原子序数为Z元素原子序数的两倍,且W与Z同主族,原子序数相差8,故Z为O,W为S,则X为Si,Y为N;
A.X为硅,位于元素周期表中第3周期第ⅣA族,A错误;
B.同周期元素的原子半径从左到右依次减小,(稀有气体除外),同主族元素的原子半径从上到下依次增大,故半径:r(X)>r(Y)>r(Z),B正确;
C.SiO2为原子晶体,NO2为分子晶体,SiO2为酸性氧化物,而NO2不是酸性氧化物,所以二者的结构和化学性质均不相似,C错误;
D.比较元素非金属性的强弱时应比较其最高价氧化物对应的水化物的酸性强弱,D错误;
综上所述,本题选B。

练习册系列答案
相关题目