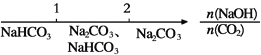题目内容
【题目】在t ℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )

A. t ℃时,Ag2CrO4的Ksp为1×10-8
B. 饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C. t ℃时,Y点和Z点时Ag2CrO4的Ksp相等
D. t ℃时,将0.1 mol·L-1 AgNO3滴入20 mL 0.1 mol·L-1 KCl和0.1 mol·L-1 K2CrO4的溶液中,Cl-先沉淀
【答案】A
【解析】根据图像可知,曲线上的点是沉淀溶解平衡点,Ag2CrO4(s)![]() 2Ag++CrO42-,Ksp=c(Ag+)2 c(CrO42-)=(10-3)2×10-5=10-11, A错误;饱和Ag2CrO4溶液中加入K2CrO4,溶液仍为饱和溶液,点仍然在曲线上,不能使溶液由Y点变为X点,B正确;Ksp是温度的函数,t ℃时,Y点和Z点时Ag2CrO4的Ksp相等,C正确;根据溶度积进行计算:Ksp(Ag2CrO4)=10-11,Ksp(AgCl)=1.8×10-10;c(CrO42-)=0.1 mol·L-1,得到c(Ag+)2=10-10,c(Ag+)=10-5 mol·L-1 ;0.1 mol·L-1 KCl溶液中,c(Cl-)=0.1 mol·L-1,根据溶度积进行计算,c(Ag+)=1.8×10-9 mol·L-1,所以氯化银先析出,Cl-先沉淀,D正确;正确选项A。
2Ag++CrO42-,Ksp=c(Ag+)2 c(CrO42-)=(10-3)2×10-5=10-11, A错误;饱和Ag2CrO4溶液中加入K2CrO4,溶液仍为饱和溶液,点仍然在曲线上,不能使溶液由Y点变为X点,B正确;Ksp是温度的函数,t ℃时,Y点和Z点时Ag2CrO4的Ksp相等,C正确;根据溶度积进行计算:Ksp(Ag2CrO4)=10-11,Ksp(AgCl)=1.8×10-10;c(CrO42-)=0.1 mol·L-1,得到c(Ag+)2=10-10,c(Ag+)=10-5 mol·L-1 ;0.1 mol·L-1 KCl溶液中,c(Cl-)=0.1 mol·L-1,根据溶度积进行计算,c(Ag+)=1.8×10-9 mol·L-1,所以氯化银先析出,Cl-先沉淀,D正确;正确选项A。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】Ⅰ、元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_________。
(2)+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的Cr2O72还原成Cr3+,该反应的离子方程式为______________。
Ⅱ、以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
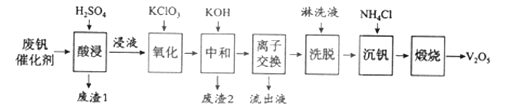
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________
(2)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
III、氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有Fe(Ⅱ), Mn(Ⅱ), Ni(Ⅱ)等杂质)的流程如下:

在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2,回答下列问题:
反应②中发生反应的离子方程式为___________,___________。