题目内容
【题目】金刚石、石墨、C60和石墨烯都是碳的同素异形体,其结构示意图如下:

(1)石墨晶体中存在的作用力有________________________________
(2)金刚石质硬但脆,金刚石能被砸碎的原因是___________________________;金刚石、石墨、C60的熔点由高到低的顺序是________________________。
(3)C60晶体的堆积方式为______________;晶体中C60的配位数为_________。
(4)石墨烯具有神奇的特性,两位科学家由于对石墨烯研究做出重大贡献而获得了2010年诺贝尔物理学奖。石墨烯即单层石墨。石墨烯中碳原子的杂化轨道类型为_______________;碳碳键的键角是_________;碳原子和碳碳键的个数比是_______;12g石墨烯中含有________个六元环。
(5)碳化硅的结构与金刚石类似,设碳化硅的密度为a g/cm3,碳化硅晶体内碳硅键的键长为______pm(用NA表示阿伏加德罗常数的值,列表达式即可)。
【答案】 共价键、金属键、范德华力 共价键具有方向性,当受到大的外力作用会发生原子间错位而断裂 石墨、金刚石、C60 面心立方堆积或分子密堆积 12 sp2 1200 2:3或2/3 3.01×1023 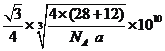
【解析】(1)石墨晶体中层内C-C键为共建键,层与层之间为范德华力和金属键。
(2)金刚石中只存在C-C共价键, 共价键具有方向性,当受到大的外力作用会发生原子间错位而断裂。金刚石属于原子晶体,石墨片层内以共价键结合,片层之间以分子间作用力结合,为混合晶体,C60属于分子晶体,他们的熔点由高到低的顺序是石墨、金刚石、C60。
(3)C60晶体组成微粒为60个碳原子组成的C60分子,属于分子晶体,堆积方式为面心立方堆积或分子密堆积。晶体中C60的配位数12。
(4)石墨烯为片层结构,杂化类型为![]() 杂化, 碳碳原子之间形成六元环键角是120
杂化, 碳碳原子之间形成六元环键角是120![]() 因此,本题正确答案是:;
因此,本题正确答案是:;![]() ; 每个碳原子被三个六圆环共用,每条键被两个六元环共用,所以碳原子和碳碳键的个数比是2:3。每个六元环含有(6
; 每个碳原子被三个六圆环共用,每条键被两个六元环共用,所以碳原子和碳碳键的个数比是2:3。每个六元环含有(6![]() )个碳原子,所以12g石墨烯中含有3.01×1023个六元环。
)个碳原子,所以12g石墨烯中含有3.01×1023个六元环。
(5)金刚石结构是一种由两个面心立方点阵沿立方晶胞的体对角线偏移1/4单位嵌套而成的晶体结构,属于面心立方体系,碳化硅的结构与金刚石类似,因为碳化硅的密度为a g/cm3,根据计算密度公式先求碳化硅的质量,再求面心立方体,通过计算知碳化硅晶体内碳硅键的键长为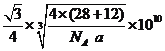

 字词句段篇系列答案
字词句段篇系列答案【题目】下列实验的叙述中有错误的是
选项 | 实验操作 | 目的或结论 |
A | 向2mL滴有2滴KSCN溶液的FeI2溶液中加入几滴氯水 | 确定Fe2+、I-还原性的相对强弱 |
B | 将C2H5OH与浓H2SO4在蒸馏烧瓶中混合后加热至170℃,将从瓶内逸出的物质通入到酸性KMnO4溶液中 | 检验有无乙烯生成 |
C | 将含有CO的CO2缓慢通过灼热的CuO | 除去CO |
D | 用一定浓度的NaOH滴定一定体积、浓度的草酸(H2C2O4、弱酸)溶液(用酚酞作指示剂) | 确定草酸是二元酸 |
A. A B. B C. C D. D