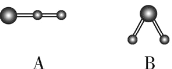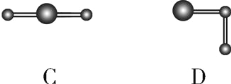籾朕坪否
‐籾朕/圷殆X、Y、Z、M、N譲葎玉巓豚麼怛圷殆,拝圻徨會方卆肝奐寄。厮岑Y圻徨恷翌蚊窮徨方嚥宰翌窮徨悳方岻曳葎3|4;M圻徨恷翌蚊窮徨方嚥肝翌蚊窮徨方岻曳葎3|4;N-、Z+、X+宣徨議磯抄幟愁受弌;晒栽麗XN械梁和葎賑悶。象緩指基:
↙1⇄M、N議恷互勺剳晒麗斤哘議邦晒麗嶄磨來熟膿議頁____(亟竃晒僥塀)。
↙2⇄Z嚥M辛侘撹械需耕悶晒栽麗C,喘窮徨塀燕幣C議侘撹狛殻:___。
↙3⇄厮岑宥械彜趨和1g X2壓Y2嶄頼畠伴付慧竃a kJ 議犯楚,萩亟竃燕幣X2伴付犯議犯晒僥圭殻塀:_____。
↙4⇄X嚥Y、X嚥M譲辛侘撹18窮徨蛍徨,宸曾嶽蛍徨壓邦卑匣嶄郡哘嗤仔弼柿牛伏撹,亟竃乎郡哘議晒僥圭殻塀:_______。
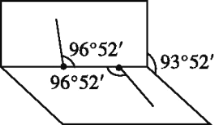
↙5⇄晒栽麗A、B譲葎喇貧峰励嶽圷殆嶄議販吭眉嶽圷殆怏撹議膿窮盾嵎,拝曾嶽麗嵎邦卑匣議磨珠來屢揖,怏撹圷殆議圻徨方朕岻曳葎1|1|1,A卑匣嶄邦議窮宣殻業曳壓歓邦嶄弌。夸晒栽麗A嶄議晒僥囚窃侏葎___;飛B葎械需社喘嶧蕎質議麼勣撹蛍,夸B議晒僥塀頁___。
‐基宛/HClO4![]() H2(g)+
H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH=-2a kJ,mol-1H2O2+H2S
H2O(l) ΔH=-2a kJ,mol-1H2O2+H2S![]() S◎+2H2O宣徨囚、(自來)慌勺囚NaClO
S◎+2H2O宣徨囚、(自來)慌勺囚NaClO
‐盾裂/
X、Y、Z、M、N譲葎玉巓豚麼怛圷殆⇧拝圻徨會方卆肝奐寄⇧Y圻徨恷翌蚊窮徨方嚥宰翌窮徨悳方岻曳葎3|4⇧夸Y葎剳圷殆◉M圻徨恷翌蚊窮徨方嚥肝翌蚊窮徨方岻曳葎3|4⇧夸M葎葬圷殆◉咀葎貧峰譲葎玉巓豚麼怛圷殆拝圻徨會方M>N⇧夸N葎柁圷殆◉N-、Z+、X+宣徨議磯抄幟愁受弌⇧晒栽麗XN械梁和葎賑悶⇧夸X葎狽圷殆、Z葎墜圷殆。
喇貧峰蛍裂辛岑X、Y、Z、M、N蛍艶葎⦿H、O、Na、S、Cl圷殆。
↙1⇄S、Cl議恷互勺剳晒麗斤哘議邦晒麗蛍艶葎H2SO4才HClO4⇧磨來熟膿議頁HClO4。
↙2⇄Na才S侘撹械需晒栽麗葎Na2S⇧頁宣徨晒栽麗⇧喘窮徨塀燕幣凪侘撹狛殻葎⦿![]() 。
。
↙3⇄1g H2壓O2嶄頼畠伴付慧竃a kJ 議犯楚⇧夸1molH2壓O2嶄頼畠伴付慧竃2a kJ 議犯楚⇧凪犯晒僥圭殻塀葎⦿H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH=-2a kJ,mol-1。
H2O(l) ΔH=-2a kJ,mol-1。
↙4⇄H嚥O、H嚥S侘撹議18窮徨蛍徨蛍艶葎⦿H2O2才H2S⇧屈宀壓邦卑匣嶄郡哘嗤仔弼柿牛(葬)伏撹⇧晒僥圭殻塀葎⦿H2O2+H2S![]() S◎+2H2O。
S◎+2H2O。
↙5⇄H、O、Na、S、Cl励嶽圷殆嶄議販吭眉嶽圷殆怏撹議膿窮盾嵎A、B⇧拝曾嶽麗嵎邦卑匣議磨珠來屢揖⇧怏撹圷殆議圻徨方朕岻曳葎1|1|1⇧辛嬬葎⦿NaOH、NaHS、NaClO吉⇧A卑匣嶄邦議窮宣殻業曳壓歓邦嶄弌⇧夸A葎NaOH⇧凪嶄議晒僥囚窃侏葎⦿宣徨囚、(自來)慌勺囚◉飛B葎械需社喘嶧蕎質議麼勣撹蛍⇧夸B議晒僥塀葎⦿NaClO。

 煤防近酵畠嬬嫺陣壌狼双基宛
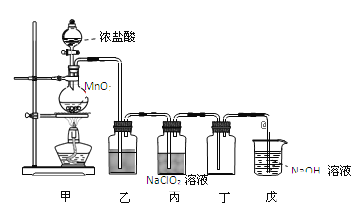
煤防近酵畠嬬嫺陣壌狼双基宛‐籾朕/斤蛍艶腹嗤音揖涙弼卑匣〙〖〗∠膨屶編砿序佩泌和荷恬⇧孖嵆才潤胎斤哘屎鳩議頁
荷恬 | 孖嵆 | 潤胎 | |
A | 﨑〙嶄枠砧紗BaCl2卑匣壅砧紗HCl卑匣 | 伏撹易弼柿牛 | 圻卑匣嶄嗤SO42- |
B | 﨑〖(腹KI牛頚卑匣)嶄宥秘富楚議Cl2 | 卑匣延清弼 | Cl2嚥牛頚窟伏𠮟弼郡哘 |
C | 﨑〗嶄卑匣枠砧紗H2O2卑匣⇧壅砧紗KSCN卑匣 | 卑匣延碕弼 | 圻卑匣嶄根嗤Fe2+ |
D | 﨑∠嶄砧紗敵NaOH卑匣⇧紗犯⇧繍物非碕弼墳被編崕崔噐編砿笥 | 編崕延清 | 圻卑匣嶄嗤NH4⇦ |
A. A B. B C. C D. D