题目内容
(7分)金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:
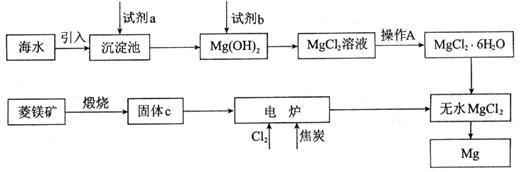
回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)

回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
(1)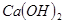 (1分,
(1分,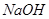 、
、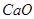 均可)
均可)
(2)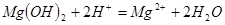 (2分)(不配平扣1分)
(2分)(不配平扣1分)
(3)过滤(1分,“滤”字错不得分)
(4)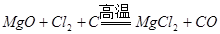 (2分,条件不扣分)
(2分,条件不扣分)
(5)电解 产生的
产生的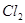 可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。(1分,任答一点即可,其他合理答案给分)
可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。(1分,任答一点即可,其他合理答案给分)
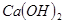 (1分,
(1分,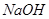 、
、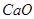 均可)
均可)(2)
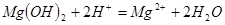 (2分)(不配平扣1分)
(2分)(不配平扣1分)(3)过滤(1分,“滤”字错不得分)
(4)
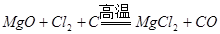 (2分,条件不扣分)
(2分,条件不扣分)(5)电解
 产生的
产生的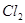 可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。(1分,任答一点即可,其他合理答案给分)
可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。(1分,任答一点即可,其他合理答案给分)(1)要沉淀溶液中的镁离子,需要加入氢氧化钙,则a是氢氧化钙。
(2)要使氢氧化镁生成氯化镁,需要加入盐酸,方程式为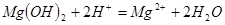 。
。
(3)析出晶体后,过滤即可。
(4)n(Cl2):n(焦炭)=1:1,则根据电子得失守恒可知,C的氧化产物使CO,所以方程式为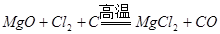 。
。
(5)考查环境保护,资源合理利用等,答案是电解 产生的
产生的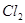 可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。
可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。
(2)要使氢氧化镁生成氯化镁,需要加入盐酸,方程式为
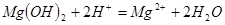 。
。(3)析出晶体后,过滤即可。
(4)n(Cl2):n(焦炭)=1:1,则根据电子得失守恒可知,C的氧化产物使CO,所以方程式为
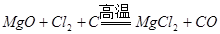 。
。(5)考查环境保护,资源合理利用等,答案是电解
 产生的
产生的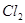 可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。
可循环利用(用于制盐酸或者在电炉中循环反应);电炉中生成的CO可燃烧,用于提供煅烧菱镁矿所需的热量。
练习册系列答案
相关题目
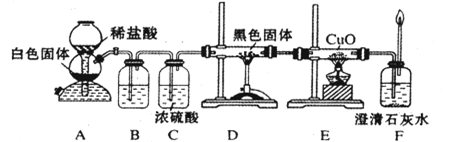
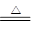 CO+H2 CO + H2O
CO+H2 CO + H2O 2CO
2CO 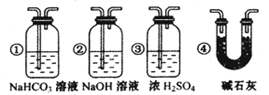
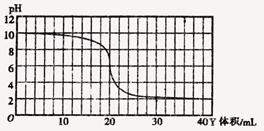

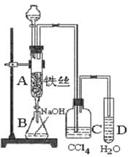
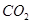 发生装置(X)的气密性,请写出主要操作过程:
发生装置(X)的气密性,请写出主要操作过程: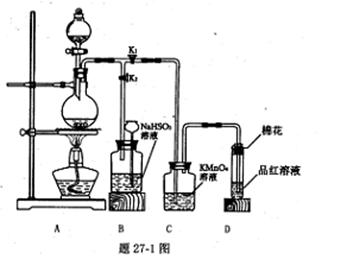
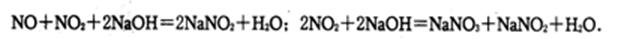
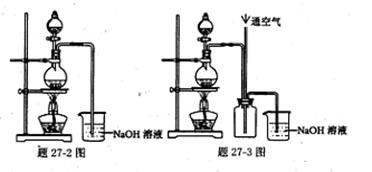
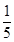 ,保留小数点后一位,并忽略装置中原有空气的影响)
,保留小数点后一位,并忽略装置中原有空气的影响)