题目内容
块状CaCO3、粉末状CaCO3与0.1mol/L的盐酸反应,谁快谁慢?为什么?
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:对于碳酸钙与盐酸的反应来说,固体表面积越大,、溶液浓度越大,以及反应的温度越高,则反应速率越大,以此解答.
解答:
解:粉末状CaCO3固体表面积较大,与盐酸反应时,接触面积较大,则反应速率较大,
答:粉末状CaCO3;固体表面积越大,反应速率越大.
答:粉末状CaCO3;固体表面积越大,反应速率越大.
点评:本题考查影响化学反应速率的因素,把握温度、浓度、接触面积影响反应速率即可解答,注意相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
甲、乙、丙三个烧杯内分别盛放0.1mol的钠、氧化钠和氢氧化钠,然后加入100mL水,搅拌,使固体完全溶解,则三份溶液的质量分数大小的顺序是( )
| A、甲<乙<丙 |
| B、丙<甲<乙 |
| C、甲=丙<乙 |
| D、丙<甲=乙 |
下列各组物质既不属于同位素,也不属于同素异形体的是( )
| A、16O和18O |
| B、金刚石、石墨和富勒烯(C60) |
| C、O2和O3 |
| D、H2O和H2O2 |
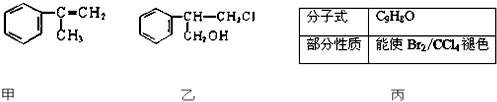
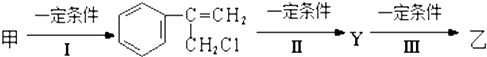
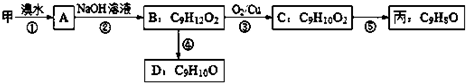
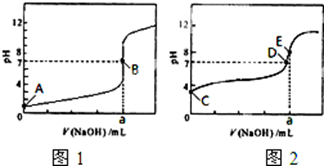 (1)常温下,用0.1000mol?L-1 NaOH溶液分别滴定20.00mL 0.1000mol?L-1 HCl溶液和20.00mL 0.1000mol?L-1 CH3COOH溶液,得到2条滴定曲线,如图所示.
(1)常温下,用0.1000mol?L-1 NaOH溶液分别滴定20.00mL 0.1000mol?L-1 HCl溶液和20.00mL 0.1000mol?L-1 CH3COOH溶液,得到2条滴定曲线,如图所示.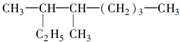 的名称是
的名称是