题目内容
20.(1)合理选用食品可以调节人体体液的酸碱平衡,蛋白质属于酸性(填“酸性”或“碱性”,下同)食品,菜蔬、水果属于碱性食品.(2)炒过菜的铁锅未及时洗净,不久便会出现红色锈斑.铁锅的锈蚀主要属于吸氧(填“析氢”或“吸氧”)腐蚀,其电池反应正极的电极反应式为O2+2H2O+4e-=4OH-.
分析 (1)食物的酸碱性与化学上所指的溶液的酸碱性是不同的概念,它是指食物的成酸性或成碱性,是按食物在体内代谢最终产物的性质来分类的;
(2)中性或弱酸性条件下,钢铁发生吸氧腐蚀.
解答 解:(1)蛋白质属于酸性食品,而水果属于碱性食品,故答案为:酸性;碱性;
(2)弱酸或中性条件下,钢铁发生吸氧腐蚀;铁、碳和电解质溶液构成原电池,铁作负极,碳作正极,正极上氧气得电子发生还原反应,电极反应式为:2H2O+O2+4e-=4OH-,故答案为:吸氧;O2+2H2O+4e-=4OH-.
点评 本题考查食物的酸碱性以及金属腐蚀等,是一道综合题,电极反应式的书写是解题的难点,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
11.对于锌、铜和稀硫酸组成的原电池,下列有关说法正确的是( )
| A. | Zn是正极 | B. | 电子由铜片经外电路流向锌片 | ||
| C. | Zn-2e-═Zn2+ | D. | 溶液中H+向锌片迁移 |
8.下列说法正确的是( )
| A. | 钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀 | |
| B. | 原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀 | |
| C. | 钢铁电化学腐蚀的两种类型主要区别在于水膜的pH不同,引起的负极反应不同 | |
| D. | 无论哪种类型的腐蚀,其实质都是金属被氧化 |
15.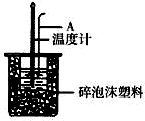 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方式NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
(2)如右图所示,仪器A的名称是环形玻璃搅拌棒;大小烧瓶间填满泡沫塑料的作用减少实验过程中的热量损失.
(3)假设盐酸和NaOH溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18×10-3kJ/(g•℃).
为了计算中和热,某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热△H=-51.8kJ/mol;(结果保留一位小数)
(4)上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)ac.
a.实验装置保温、隔热效果差
b.把NaOH溶液迅速倒入盛有稀硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的.
 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方式NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
(2)如右图所示,仪器A的名称是环形玻璃搅拌棒;大小烧瓶间填满泡沫塑料的作用减少实验过程中的热量损失.
(3)假设盐酸和NaOH溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18×10-3kJ/(g•℃).
为了计算中和热,某学生实验记录数据如下:
| 实验序号 | 起始温度t1℃ | 终止温度t1℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
(4)上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)ac.
a.实验装置保温、隔热效果差
b.把NaOH溶液迅速倒入盛有稀硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的.
5.下列解释实验事实的离子方程式不正确的是( )
| A. | 氧化铝与稀盐酸:Al2O3+6 H+═2 Al3++3H2O | |
| B. | 稀H2SO4与BaCl2溶液反应生成沉淀:Ba2++SO42-═BaSO4↓ | |
| C. | 用大理石与稀盐酸制备CO2:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯气与氯化亚铁溶液:Cl2+Fe2+═2Cl-+Fe3+ |
9.下列说法正确的是( )
| A. | 能够发生化学反应的碰撞是有效碰撞 | |
| B. | 活化分子之间的碰撞一定是有效碰撞 | |
| C. | 反应物分子的每次碰撞都能发生化学反应 | |
| D. | 增大反应物浓度时,活化分子百分数增大 |
11.判断下列有关化学基本概念的依据正确的是( )
| A. | 氧化还原反应:元素化合价是否变化 | |
| B. | 碱性氧化物:是否是金属氧化物 | |
| C. | 电解质和非电解质:溶于水或熔融状态下能否导电 | |
| D. | 同素异形体:是否由同一种原子构成 |