题目内容
7.某种分子的球棍模型如图所示(图中球与球之间的连线可代表单键、双键、叁键等):不同形式的球代表不同的原子,对该物质的判断正确的是( )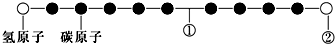
| A. | ①处的化学键是碳碳双键 | |
| B. | ②处的原子可能是氯原子 | |
| C. | 该分子中的原子不可能均在同一直线上 | |
| D. | 该分子不存在链状同分异构体 |
分析 碳原子能够形成四个共价键,氢原子能够形成1个共价键,所以从左到右碳碳键分别为C-H、C≡C、C-C、C≡C、C-C、C≡C、C-C、C≡C、C-C、C-H键,以此解答.
解答 解:碳原子能够形成四个共价键,氢原子能够形成1个共价键,所以从左到右碳碳键分别为C-H、C≡C、C-C、C≡C、C-C、C≡C、C-C、C≡C、C-C、C-H键,则
A.①处的化学键C≡C键,故A错误;
B.②处的原子应是H原子,如是氯原子,半径比碳原子半径大,故B错误;
C.含有C≡C结构,为直线形,故C错误;
D.碳原子能够形成四个共价键,分子中不可能存在C≡C≡C的结构,则一定只能为-C≡C-C-C≡C-C-结构,且不存在链状同分异构体,故D正确;
故选D.
点评 本题考查有机物结构与性质,试题难度中等,是对学生综合能力的考查与知识的运用,解题关键是根据有机物中碳原子形成的共价键数目推断有机物中存在的化学键,试题考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.从能量的变化和反应的快慢等角度研究反应:2H2+O2═2H2O.
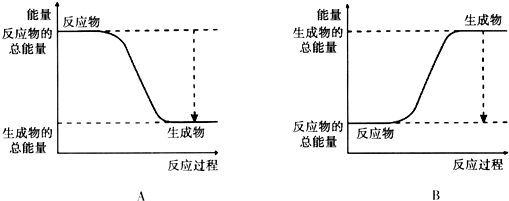
(1)已知该反应为放热反应,下图能正确表示该反应中能量变化的是A.
(2)从断键和成键的角度分析上述反应中能量的变化.已知:化学键的键能:
由此计算2mol H2在氧气中燃烧生成气态水放出的热量484kJ
(3)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为2H2 (g)+O2(g)=2H2O(l)△H=-4QKJ/mol
(4)氢氧燃料电池的总反应方程式为2H2+O2═2H2O.电路中每转移0.2mol电子,标准状况下消耗H2的体积是2.24L.
(1)已知该反应为放热反应,下图能正确表示该反应中能量变化的是A.

(2)从断键和成键的角度分析上述反应中能量的变化.已知:化学键的键能:
| 化学键 | H-H | O=O | H-O |
| 键能kJ•mol-1 | 436 | 496 | 463 |
(3)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为2H2 (g)+O2(g)=2H2O(l)△H=-4QKJ/mol
(4)氢氧燃料电池的总反应方程式为2H2+O2═2H2O.电路中每转移0.2mol电子,标准状况下消耗H2的体积是2.24L.
15.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,2.24L 氯气与氢氧化钠溶液完全反应转移的电子数为0.1NA | |
| B. | 标准状况下,1L辛烷完全燃烧后,所生成气体产物的分子数为8NA/22.4 | |
| C. | 0.1L 2mol•L-1的(NH4)2S溶液中含有的S2-数目为0.2 NA | |
| D. | 在含有4mol Si-O键的石英晶体中,氧原子的数目为2NA |
19.下列各组物质中,既不是同系物,又不是同分异构体的是( )
| A. | CH4和C4H10 | B. | 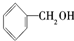 和 和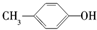 | C. | 乙酸和甲酸甲酯 | D. | 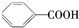 和 和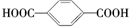 |
16.下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
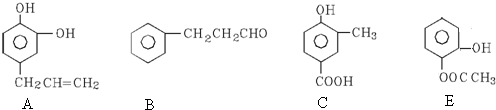
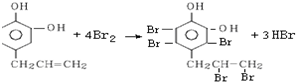 .
.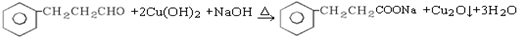 .
.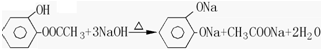 .
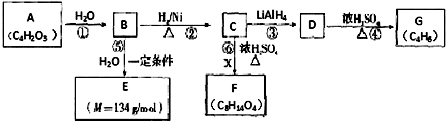
.
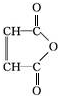 .
. .
.