题目内容
下列各组离子能大量共存的是
| A.加入KSCN显红色的溶液中:K+、NH4+、Cl―、I― |
| B.含“84”消毒夜(有效成分NaClO)的溶液中:Fe2+、Cl―、Ca2+、Na+ |
| C.常温下,pH=1的溶液中:NH4+、Na+、Cl―、Cu2+ |
| D.常温下,pH=13的无色溶液中:K+、NO3―、HCO3―、Al3+ |
C
解析试题分析:Fe3+遇KSCN溶液变红,则加入KSCN显红色的溶液中一定大量存在Fe3+,由于2Fe3++2I―=2Fe2++I2,具有强氧化性的Fe3+与强还原性的I―不能大量共存,故A错误;ClO―具有强氧化性,Fe2+具有强还原性,二者容易发生氧化反应反应,生成Cl―和Fe3+,故B错误;常温下pH=1的溶液中大量存在H+,H+、NH4+、Na+、Cl―、Cu2+之间不能反应,故C正确;常温下pH=13的溶液中大量存在OH―,OH―与HCO3―容易发生中和反应,生成H2O和CO32―,OH―与Al3+容易发生复分解反应,生成Al(OH)3或AlO2―和H2O,故D错误。
考点:考查离子共存,涉及铁离子的显色反应和氧化还原反应、亚铁离子的氧化还原反应、溶液的酸碱性和pH、碳酸氢根离子的酸性、铝离子的沉淀反应或铝三角的转化等。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是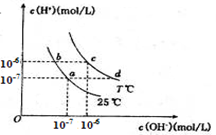
| A.a点对应的无色溶液中能大量存在:Fe3+、Na+、Cl-、SO42- |
| B.b点对应的溶液中能大量存在:NH4+、Ca2+、AlO2-、I- |
| C.c点对应的溶液中能大量存在:Na+、Ba2+、Cl-、CO32- |
| D.d点对应的溶液中能大量存在:Na+、K+、SO32-、Cl- |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1mo1/L NaI溶液:K+、Na+、MnO4-、OH- |
| B.能溶解CaCO3的溶液:K+、NH4+、Cl-、NO3- |
| C.0.1mo1/LNaHSO3溶液:Na +、Mg2+、SO42-、ClO- |
| D.c(H+)/c(OH-)=1013,的溶液:K+、Fe2+、Cl-、NO3- |
下列各组离子在溶液能大量共存,加入Fe2(SO4)3后仍能大量共存的是
| A.Ca2+、I-、CO32-、ClO- | B.Fe2+、H+、K+、NO3- |
| C.Ba2+、Na+、SCN-、Cl- | D.Cu2+、K+、Cl-、NO3- |
下列离子方程式中正确的是
| A.FeO溶于稀硝酸中:FeO+2H+ = Fe2++H2O |
| B.过量CO2通入NaOH溶液中:OH¯+CO2 = HCO3¯ |
| C.金属钠溶于水中:Na+H2O = Na++OH¯+H2↑ |
| D.过量氨水加入AlCl3溶液中:Al3++3OH¯= Al(OH)3↓ |
在水溶液中能大量共存的一组离子是
| A.HCO3-、H+、NO3-、Na+ | B.Na+、Cu2+、OH-、SO42- |
| C.Mg2+、H+、AlO2-、SO42- | D.NH4+、K+、Br-、NO3- |
下列离子能在水溶液中大量共存的一组是
| A.Fe3+、HCO3ˉ、Clˉ、SCNˉ | B.Ba2+、NO3ˉ、SO32ˉ、H+ |
| C.Mg2+、NH4+、Brˉ、OHˉ | D.Na+、Cu2+、SO42ˉ、Clˉ |
下列实验现象及相关的离子方程式均正确的是( )
| A.碳酸钙粉末中加入醋酸溶液,固体质量减小,生成无色气体 CaCO3 + 2H+=Ca2+ + CO2↑ + H2O |
| B.向BaCl2溶液中通入SO2气体,出现白色沉淀:Ba2+ + SO2 + H2O = BaSO3↓ + 2H+ |
| C.向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色 2MnO4- + 7H2O2 + 6H+ = 2Mn2+ + 6O2↑ + 10H2O |
| D.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,生成白色沉淀 |
(15分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3和少量的 SiO2、Fe2O3杂质)生产铵明矾晶体
NH4Al(SO4)2?12H2O,其工艺流程图如下: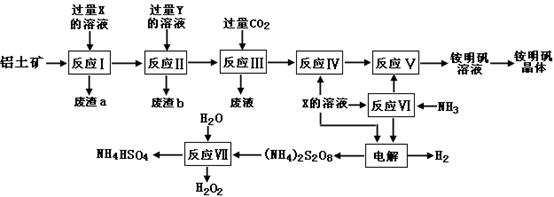
(1)废渣a、b 的成分分别是:_________、_____________。(写名称)
(2)流程图中X的化学式为:_______________。
(3)反应Ⅲ的离子方程式为:_________________________________________;从铵明矾溶液中获得铵明矾晶体的操作依次为(填操作名称)_________、冷却结晶、过滤洗涤。
(4)过硫酸铵[(NH4)2S2O8]在工业生产中有广泛的用途,可以作为氧化剂和漂白剂,广泛地用于蓄电池工业;还用作聚合的引发剂、纤维工业的脱浆剂。在上述的工艺流程中用惰性电极电解X与反应Ⅵ所得物质的混合溶液可以得到过硫酸铵。
写出阳极反应式:________________________ ____。
(5)反应Ⅶ的化学方程式为:_________________________ _____________;
NH4HSO4溶液中离子浓度由大到小顺序为:__________________________ _。
(6)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的反应是 (填选项字母)
| A.4NH4Al(SO4)2+3Ba(OH)2=2(NH4)2SO4+3BaSO4↓+ Al2 (SO4)3+2Al(OH)3↓ |
| B.2NH4Al(SO4)2+4Ba(OH)2=(NH4)2SO4+3BaSO4↓+Ba(AlO2)2 |
| C.2NH4Al(SO4)2+3Ba(OH)2=(NH4)2SO4+3BaSO4↓+2Al(OH)3↓ |
| D.NH4Al(SO4)2+2Ba(OH)2=NH3·H2O+2BaSO4↓+ Al(OH)3↓ |