题目内容
11.一定量某营养液中溶质的配方分别如下:配方一:0.3mol KCl、0.2mol K2SO4、0.1molZnSO4
配方二:0.1mol KCl、a mol K2SO4、0.1molZnCl2
对于两种营养液的成分,下列说法中不正确的是( )
| A. | 两配方中n(Cl-)相同 | |
| B. | 两配方中n(Zn2+)和a的取值无关 | |
| C. | 当a=0.3时两配方中各种离子的物质的量分别相同 | |
| D. | 当a=0.2时两配方中n(Cl-)、n(Zn2+)和n(SO42-)分别相同 |
分析 A、配方一中Cl-来自于KCl,而配方二中Cl-来自于 KCl和ZnCl2,根据各自的物质的量和化学式来计算;
B、K2SO4中不含Zn2+;
C、当a=0.3时,根据各种离子的来源来计算;
D、当a=0.2时n(SO42-)不同.
解答 解:A、配方一中Cl-来自于KCl,溶液中n(Cl-)=0.3mol;含有的额而配方二中Cl-来自于 KCl和ZnCl2,n(Cl-)=0.1mol+0.2mol=0.3mol,故A正确;
B、K2SO4中不含Zn2+,故两配方中n(Zn2+)和a的取值无关,故B正确;
C、配方一中,n(Cl-)=0.3mol,n(K+)=0.7mol,n(Zn2+)=0.1mol,n(SO42-)=0.3mol;在配方二中,当a=0.3时,n(Cl-)=0.3mol,n(K+)=0.7mol,n(Zn2+)=0.1mol,n(SO42-)=0.3mol,即各种离子的物质的量分别相同,故C正确;
当a=0.3时,根据各种离子的来源来计算;
D、配方一中,n(SO42-)=0.3mol,而当a=0.2时,配方二中,n(SO42-)=0.2mol,故D错误.
故选D.
点评 本题综合考查物质的量,为高频考点,侧重学生的分析能力和计算能力的考查,注意物质的构成特点,难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
1.下列离子方程式书写正确的是( )
| A. | 向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | NH4HSO3溶液与足量NaOH溶液反应:HSO3-+OH-═SO32-+H2O | |
| C. | Fe(OH)2溶于稀HNO3:Fe(OH)2+2H+═Fe2++2H2O | |
| D. | H218O2中加入H2SO4酸化的KMnO4 5H218O2+2MnO4-+6H+═518O2+2Mn2++8H2O |
2.下列说法中正确的是( )
| A. | 不能发生丁达尔效应的分散系有氯化钠溶液、水等 | |
| B. | 根据分散系的稳定性,将分散系分为胶体、浊液和溶液 | |
| C. | 可吸入颗粒(如硅酸盐粉尘)能形成气溶胶,对人类的健康危害极大 | |
| D. | FeCl3溶液与Fe(OH)3胶体的本质区别是有无丁达尔效应 |
20.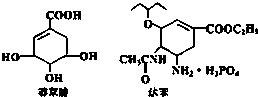 2005年禽流感在全球蔓延,百姓谈“禽”色变.目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物.下列有关描述正确的是( )
2005年禽流感在全球蔓延,百姓谈“禽”色变.目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物.下列有关描述正确的是( )
 2005年禽流感在全球蔓延,百姓谈“禽”色变.目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物.下列有关描述正确的是( )
2005年禽流感在全球蔓延,百姓谈“禽”色变.目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物.下列有关描述正确的是( )| A. | 莽草酸、达菲都属于芳香族化合物 | |
| B. | 莽草酸既能发生加成反应,又能发生取代反应 | |
| C. | 莽草酸、达菲都能使溴水或酸性KMnO4溶液褪色 | |
| D. | 1mol达菲与NaOH溶液反应,消耗NaOH的物质的量最多为3mol |