题目内容
15.下列反应中,其中反应物的总能量高于生成物的总能量的是( )①NaOH溶液中加入盐酸 ②由乙醇制C2H4 ③铝热反应 ④由氯酸钾制O2.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①④ |
分析 反应中反应物总能量高于生成物总能量,说明该反应是一个放热反应,常见放热反应有大多数化合反应、酸碱中和反应、金属与酸的反应,物质的燃烧等,常见吸热反应有大多数分解反应,C、CO等还原剂与金属氧化物的反应,Ba(OH)2•8H2O与NH4Cl反应等,以此解答.
解答 解:①NaOH溶液中加入盐酸为中和反应属于放热反应;②由乙醇制C2H4属于吸热反应;③铝热反应虽然要点燃镁条,但启动反应后放出大量的热,属于放热反应;④由氯酸钾制O2属于吸热反应.
故选C.
点评 本题考查了常见的吸热反应和放热反应,可以根据所学知识进行回答,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
2.3.2g某气态化合物甲在标准状况下的体积为1.12L,则甲的相对分子质量为( )
| A. | 40 g•mol-1 | B. | 22 g•mol-1 | C. | 64 | D. | 22 |
3.美丽的“水立方”(Water Cube)是北京奥运会游泳馆,采用膜材料ETFE(四氟乙烯和乙烯的共聚物),为场馆带来更多的自然光.下列说法正确的是( )
| A. | ETFE的结构中,存在-CF2-CH2-CF2-CH2-连接方式 | |
| B. | 四氟乙烯与乙烯发生缩聚反应得到ETFE | |
| C. | 以乙烯为原料经过加成反应、取代反应可制得乙二醇 | |
| D. | ETFE材料是热固型(体形结构)的塑料 |
10.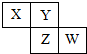 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
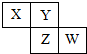 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )| A. | Z单质与氢气反应较Y剧烈 | |
| B. | 最高价氧化物对应水化物酸性W比Z强 | |
| C. | X单质氧化性强于Y单质 | |
| D. | X与W的原子核外电子数相差9 |
20.在体积一定的密闭容器中进行如下反应:A2(g)+2B2(g)?2C(g),已知A2、B2、C的起始浓度分别为a mol/L、b mol/L、0.3mol/L(非平衡态),在一定条件下,当反应达到平衡时,C的浓度为 0.5mol/L,则下列判断正确的是( )
| A. | 达平衡时,A2的正反应速率与B2的逆反应速率相等 | |
| B. | b≤0.2mol/L | |
| C. | 其它条件不变,在反应过程中使用了催化剂,可提高 A2、B2的转化率 | |
| D. | 该反应达平衡时气体物质的量浓度之和小于(a+b+0.3)mol/L |
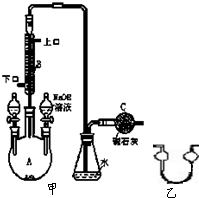 制备溴苯的实验装置如图所示,回答下列问题:
制备溴苯的实验装置如图所示,回答下列问题: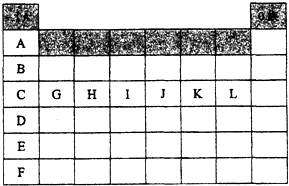 如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)
如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)