��Ŀ����
��7�֣��¹�����˹��˾�ɹ����������ü״�����������ȼ�ϵ�ع��գ���ԭ������ͼ��ʾ����۲��ͼ�ش�
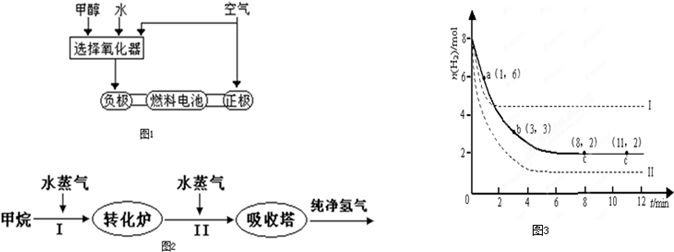
��1���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
��CH3OH��g��+H2O��g��=CO2��g��+3H2��g������H=+ 49��0 kJ��mol��1
��2CH3OH��g��+O2��g��=2CO2��g��+4H2��g������H=��385.8kJ��mol��1
����˵����ȷ����
A����Ӧ���з�Ӧ��������������������������
B����Ӧ���в�CH3OH��g����H2O��g���еĻ�ѧ���������������γ�CO2��g����3H2��g�� �еĻ�ѧ�����ͷŵ�����
C��CH3OH������ȼ����Ϊ����192��9 kJ��mol��1
D�����ݢ���֪��Ӧ��2CH3OH��l��+ O2��g��=2CO2��g��+4H2��g���ġ�H����385��8kJ��mol��1
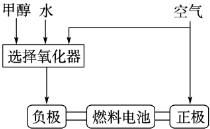
��2�������ѧ���������ɫ���ɡ����룺�ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��ʹ�����е�CO2ת��Ϊ������ȼ�ϼ״�������2.2kg CO2������H2ǡ����ȫ��Ӧ��������̬��ˮ�ͼ״����ɷų�2473.5 kJ����������д���ϳ����з�����Ӧ���Ȼ�ѧ����ʽ ��
��3���ɸ��ʼDZ����Թ���ļ״�ȼ�ϵ���Ѿ���������ṹʾ��ͼ����ͼ���״��ڴ����������ṩ���ӣ�H�����͵��ӣ����Ӿ����·�����Ӿ��ڵ�·������һ�缫����������Ӧ������ܷ�ӦΪ��2CH3OH��3O2=2CO2��4H2O��b��ͨ��������� ��������ӦΪ�� ��
��1�� BC D ��2�֣�
��2��CO2��g��+ 3H2��g��= H2O��g��+CH3OH��g�� ��H=-49.47kJ/mol��2�֣�
��3����������� 1�� CH3OH��H2O��6e��=CO2��6H�� 2��
����:

 �¹�����˹��˾�ɹ����������ü״�����������ȼ�ϵ�ع��գ���ԭ����ͼ1��ʾ����۲��ͼ�ش�
�¹�����˹��˾�ɹ����������ü״�����������ȼ�ϵ�ع��գ���ԭ����ͼ1��ʾ����۲��ͼ�ش�