题目内容
下表为元素周期表的一部分,请参照元素A-H在表中的位置,用化学用语回答下列问题:
(1)上述元素中非金属性最强的元素是______,金属性最强的是______.
(2)B、C、H的最高价含氧酸的酸性由强到弱的顺序是______.D、E、F的原子半径由大到小的顺序为______.
(3)上述一元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式______;
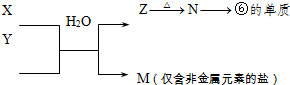
(4)上述某元素的单质在常温下为气态,该元素能与A-H中一种元素构成原子个数比为1:1和1:2的两种共价化合物X、Y,还能与A-H中另一种元素构成原子个数比为1:1和1:2的两种离子化合物化合物Z、M,回答下列问题:
①写出物质X的电子式______;
②写出Z与Y反应的化学方程式______.
| 族 周期 |
IA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | B | C | D | E | ||||
| 3 | F | G | H | |||||
(2)B、C、H的最高价含氧酸的酸性由强到弱的顺序是______.D、E、F的原子半径由大到小的顺序为______.
(3)上述一元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式______;
(4)上述某元素的单质在常温下为气态,该元素能与A-H中一种元素构成原子个数比为1:1和1:2的两种共价化合物X、Y,还能与A-H中另一种元素构成原子个数比为1:1和1:2的两种离子化合物化合物Z、M,回答下列问题:
①写出物质X的电子式______;
②写出Z与Y反应的化学方程式______.
由元素所在周期表中的位置可知,A为H元素,B为C元素,C为N元素,D为O元素,E为F元素,F为Na元素,G为Al元素,H为Si元素,则
(1)非金属性最强的元素为F,金属性最强的元素为Na,故答案为:F;Na;
(2)由于非金属性:N>C>Si,则对应的最高价氧化物的水化物的酸性:HNO3>H2CO3>H2SiO3,原子的核外电子层数越多,半径越大,Na原子核外有3个电子层,原子半径最大,同周期元素的原子序数越大,半径越小,则原子半径O>F,所以半径:Na>O>F,
故答案为:HNO3>H2CO3>H2SiO3;Na>O>F;
(3)上述一元素能形成两性氧化物为Al2O3,与强碱反应生成偏铝酸盐和水,反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(4)对应的化合物分别是:X:H2O2,Y:H2O,Z:Na2O2,M:Na2O,
①H2O2的电子式为
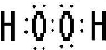
,故答案为:
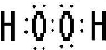
;
②Na2O2和水反应生成NaOH和氧气,反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,
故答案为:2Na2O2+2H2O═4NaOH+O2↑.
(1)非金属性最强的元素为F,金属性最强的元素为Na,故答案为:F;Na;
(2)由于非金属性:N>C>Si,则对应的最高价氧化物的水化物的酸性:HNO3>H2CO3>H2SiO3,原子的核外电子层数越多,半径越大,Na原子核外有3个电子层,原子半径最大,同周期元素的原子序数越大,半径越小,则原子半径O>F,所以半径:Na>O>F,
故答案为:HNO3>H2CO3>H2SiO3;Na>O>F;
(3)上述一元素能形成两性氧化物为Al2O3,与强碱反应生成偏铝酸盐和水,反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(4)对应的化合物分别是:X:H2O2,Y:H2O,Z:Na2O2,M:Na2O,
①H2O2的电子式为
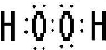
,故答案为:
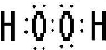
;
②Na2O2和水反应生成NaOH和氧气,反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,
故答案为:2Na2O2+2H2O═4NaOH+O2↑.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案
相关题目








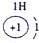
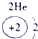
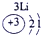
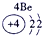
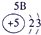
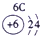
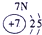
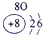
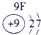
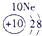
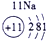





 表示的是
表示的是