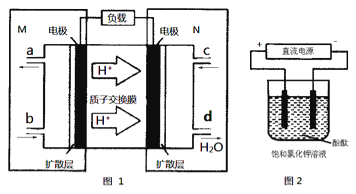
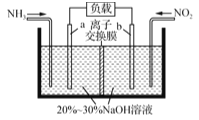
��Ŀ����
����Ŀ��ﮱ���Ϊ������ζ��������LiCoO2Ϊ��������������ӵ���ѱ��㷺������Яʽ��Դ����ҵ��������-﮻Կ�(��Ҫ�ɷ�ΪLiAlSi2O6��������FeO��MgO��CaO������)Ϊԭ������ȡ����ﮡ�����һ�ֹ���������ͼ��ʾ��
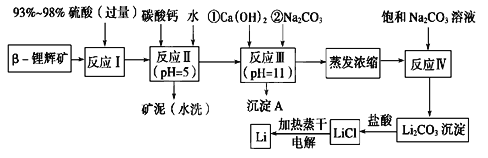
��֪�������ֽ����������↑ʼ��������ȫ����ʱ��pH���±���
�������� | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
��ʼ����pH | 2.7 | 3.7 | 9.6 |
��ȫ����pH | 3.7 | 4.7 | 11 |
��Li2CO3�ڲ�ͬ�¶��µ��ܽ�����±���
�¶�/�� | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3���ܽ��/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
��ش��������⣺
��1������������ʽ��ʾLiAlSi2O6����ɣ�________________________��
��2����Ӧ������̼�����������___________________��
��3������������ʹ��̼������Һ����˵��ǰ������ʹ����Ũ�Ȳ�ͬ��ԭ��______________��
��4��ϴ������Li2CO3����Ҫʹ��________(������ˮ��������ˮ��)����ѡ���������________________��
��5����������Li2CO3��ȫ��Ӧ�����Һ���������ɵõ����壬�ٽ��������������ﮡ����ʱ�����������л��������������ԭ���ǣ�__________________________��
��6�����й��ڽ���﮼��������˵����ȷ����___________������ţ���
A����Ǽ���������۵������ B�����ݶԽ���ԭ�����������ǿ��
C������﮵���������ʽʮ�ָ��� D����������ܶ���С����ﮣ��������
���𰸡���1��Li2O��Al2O3��4SiO2 ��2����ȥ��Ӧ���й�����H2SO4������pH��ʹFe3����Al3����ȫ����
��3����һ��Ũ�ȹ����ʹ����Li+ �������ڶ���Ũ�ȴ���������Li2CO3����������
��4����ˮ,Li2CO3�ڽϸ��¶����ܽ��С������ˮϴ�ӿɼ���Li2CO3�����
��5����������LiCl��Һʱ��LiCl������ˮ������LiOH�����ȷֽ�����Li2O�����ʱ����O2
��6��A
��������
�����������1�������μȿ������ε���ʽ��ʾ��Ҳ���������������ʽ��ʾ��������������ʽ��ʾʱҪ���������غ㶨�ɡ���һ������£�����������д��ǰ�棬�ǽ���������д�ں��档��LiAlSi2O6�����������ʽ��ʾΪLi2O��Al2O3��4SiO2��
��2����Ӧ�����̼�����Ϊ�˳�ȥ��Ӧ���й�����H2SO4������pH��ʹFe3����A l3����ȫ������
��3����һ��Ũ�ȹ����ʹ����Li+�������ڶ���Ũ�ȴ���������Li2CO3���������ɣ���������������ʹ����Na2CO3��Һ����һ��Ũ��С���ڶ���Ũ�ȴ�
��4����Ӧ��������Li2CO3�ܽ��С����������Li2CO3��������ʵ�����д���Һ�з���õ�Li2CO3�����IJ����ǹ��ˡ���ΪLi2CO3���ܽ�����¶ȵ����߶����ͣ�����ϴ������Li2CO3����Ҫʹ����ˮ��������Li2CO3�ڽϸ��¶����ܽ��С������ˮϴ�ӿɼ���Li2CO3����ġ�
��5����������Ȼ�������ʱ�����������������л����������������Ϊ�ڼ�������LiCl��Һʱ��LiCl����������ˮ�ⷴӦ����LiOH�������ȷֽ�����Li2O�����ʱ����O2�������ȡ�������г�����������O2��
��6��A����Ǽ���������۵�����ƣ�A��ȷ��B��Li��Mg���ڶԽ���λ�ã����ݶԽ���ԭ���������Ӧ�������B����C������﮵�������ֻ��һ��Li2O��C����D����������ܶ���С����ﮣ�����Ǽأ�D����ѡA��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�