题目内容
4. 某同学做如图实验,以检验反应中的能量变化.
某同学做如图实验,以检验反应中的能量变化.(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是放热反应;
(b)中温度降低,由此可以判断(b)中反应是吸热反应.
(2)根据能量守恒定律,(b)中反应物的总能量应该低于其生成物的总能量.
分析 (1)探究化学反应中的能量变化时,温度升高,则反应放热;温度降低则反应吸热;
(2)放热反应中反应物总能量高于生成物,吸热反应中反应物总能量低于生成物,据此分析.
解答 解:(1)实验中反应后(a)中温度升高,由此可以判断(a)中反应是放热反应;(b)中温度降低,由此可以判断(b)中反应是吸热反应;
故答案为:放;吸;
(2)b是吸热反应,反应物总能量低于生成物;
故答案为:低于.
点评 本题考查学生根据实验现象判断放热与吸热反应,注意放热反应反应物总能量高于生成物,吸热反应中反应物总能量低于生成物,题目难度不大.

练习册系列答案
相关题目
15.10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如表变化:
甲同学认为:该溶液pH升高的原因是HCO${\;}_{3}^{-}$的水解程度增大,碱性增强.
乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于NaHCO3的水解程度(填“大于”或“小于”).
丙同学认为甲、乙的判断都不充分.丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙(填“甲”或“乙”)的判断正确.试剂X是B.
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
(2)将加热煮沸后的溶液冷却到10℃,若溶液的pH等于8.3(填“高于”、“低于”或“等于”),则甲(填“甲”或“乙”)判断正确.
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言乙(填“甲”或“乙”)判断是错误的,理由是常压下加热NaHCO3的水溶液溶液的温度达不到150℃.
(4)关于NaHCO3饱和水溶液的表述正确的是a.
a.c(Na+)=c(HCO${\;}_{3}^{-}$)+c(CO${\;}_{3}^{2-}$)+c(H2CO3)
b.c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+c(CO${\;}_{3}^{2-}$)+c(OH-)
c.HCO${\;}_{3}^{-}$的电离程度大于HCO${\;}_{3}^{-}$的水解程度.
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
乙同学认为:该溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于NaHCO3的水解程度(填“大于”或“小于”).
丙同学认为甲、乙的判断都不充分.丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙(填“甲”或“乙”)的判断正确.试剂X是B.
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
(2)将加热煮沸后的溶液冷却到10℃,若溶液的pH等于8.3(填“高于”、“低于”或“等于”),则甲(填“甲”或“乙”)判断正确.
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言乙(填“甲”或“乙”)判断是错误的,理由是常压下加热NaHCO3的水溶液溶液的温度达不到150℃.
(4)关于NaHCO3饱和水溶液的表述正确的是a.
a.c(Na+)=c(HCO${\;}_{3}^{-}$)+c(CO${\;}_{3}^{2-}$)+c(H2CO3)
b.c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+c(CO${\;}_{3}^{2-}$)+c(OH-)
c.HCO${\;}_{3}^{-}$的电离程度大于HCO${\;}_{3}^{-}$的水解程度.
12.如何解决好碳排放问题是关系到人类可持续发展的重大课题之一.目前,采用较多的方法是对二氧化碳进行捕集封存和富集再利用.下列与二氧化碳有关的叙述正确的是( )
| A. | CO2是形成酸雨的主要物质 | |
| B. | CO2导致温室效应,是一种大气污染物 | |
| C. | CO2(g)+C(s)$\stackrel{高温}{?}$2CO(g)△H>0,高温有利于该反应自发进行 | |
| D. | 实验室常用大理石与稀盐酸或稀硫酸反应制取二氧化碳 |
9.下列离子方程式书写正确的是( )
| A. | 过量的CO2通入NaOH溶液中:CO2+2OH-=CO32 -+H2O | |
| B. | 氨水中通入过量CO2:2NH3•H2O+CO2=2NH4++CO32-+H2O | |
| C. | 饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | NaHCO3溶液中加入过量的Ca(OH)2溶液:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32 - |
13.胶体和其它分散系(溶液、浊液)的本质区别是( )
| A. | 是否有丁达尔效应 | B. | 分散质粒子的大小 | ||
| C. | 是不是稳定体系 | D. | 粒子有没有带电荷 |
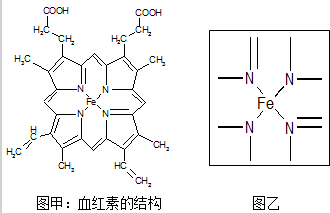
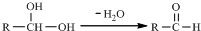 .请根据如图回答:
.请根据如图回答: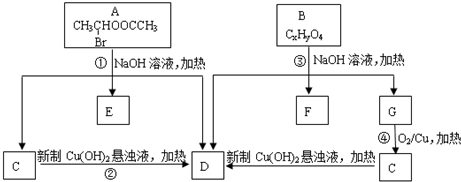
 .
. ;④
;④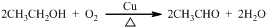 .
.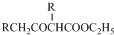 +C2H5OH
+C2H5OH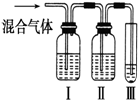 为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.