题目内容
【题目】下列反应需要加入还原剂才能发生的是( )
A.Cl→Cl2B.Fe3+→Fe2+C.SO32→SO42-D.CO32→CO2
【答案】B
【解析】
A. Cl→Cl2,Cl元素的化合价升高,被氧化,发生氧化反应,需加入氧化剂,A错误;
B. Fe3+→Fe2+,Fe元素的化合价降低,被还原,发生还原反应,需加入还原剂才能完成,B正确;
C. SO32→SO42-,S元素的化合价升高,被氧化,发生氧化反应,需加入氧化剂,C错误;
D. CO32→CO2,没有化合价的变化,不是氧化还原反应,不需要加入还原剂,D错误;故答案为:B。

 阅读快车系列答案
阅读快车系列答案【题目】某课题组以硫铁矿烧渣(含 Fe2O3、 Fe3O4、 Al2O3、 CaO、 SiO2 等)为原料制取软磁用 Fe2O3(要求纯度>99.2%, CaO 含量<0.01%)。其工艺流程如下(所加入试剂均稍过量):
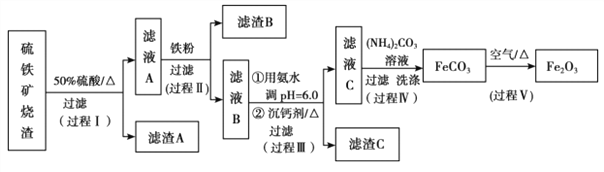
已知:生成氢氧化物的 pH 如下表所示
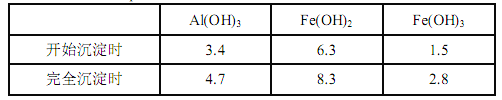
(1)滤渣 A 的主要成分是__________。
(2)在过程Ⅱ中可观察到产生少量气泡,溶液颜色慢慢变浅。能解释该实验现象的离子方程式有__________。
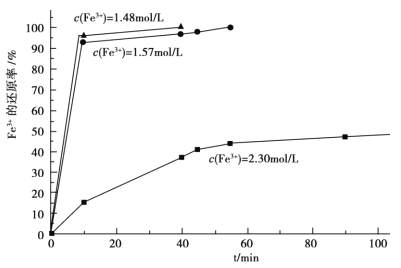
(3)在过程Ⅱ中,课题组对滤液 A 稀释不同倍数后,加入等质量的过量铁粉,得出 Fe3+浓度、还原率和反应时间的关系如图所示:结合上述实验结果说明:课题组选择稀释后c(Fe3+)为 1.60mol/L 左右的理由是______。
(4)在过程Ⅲ中,课题组在相同条件下,先选用了不同沉钙剂进行实验,实验数据见下表:(已知:滤液 B 中钙的含量以 CaO 计为 290—310mg/L)
沉钙剂 | Na2SO3 | H2C2O4 | (NH4)2CO3 | Na2CO3 | NH4F |
用量/g | 2 | 2 | 2 | 5 | 2 |
剩余CaO/mg/L) | 290 | 297 | 290 | 190 | 42 |
根据实验结果, 选择适宜的沉钙剂,得到滤渣 C 的主要成分有__________。
(5)在过程Ⅳ中,反应温度需要控制在 35℃以下,不宜过高,其可能的原因是__________。
(6)在过程Ⅴ中,反应的化学方程式是__________。