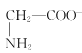题目内容
【题目】A、B、C、D是四种常见的单质,A、B为金属,C、D常温下是气体,且D为黄绿色气体。甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质。它们之间的转化关系如图所示:
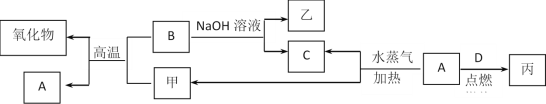
请回答下列问题:
(1)B与甲反应的化学方程式是___。
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?___(填“是”或“否”)。
(3)将丙溶于水配成溶液,检验丙中阳离子的方法所加试剂是:___。
(4)写出A与水蒸气反应生成C和甲的化学方程式___。
(5)向A、B两种金属的混合物中加入足量的NaOH溶液,发生反应的离子方程式为:___。
【答案】3Fe3O4+8Al![]() 9Fe+4Al2O3 否 取少量丙的溶液于试管中,滴加KSCN溶液,若溶液变红,说明丙中存在Fe3+ 3Fe+4H2O(g)
9Fe+4Al2O3 否 取少量丙的溶液于试管中,滴加KSCN溶液,若溶液变红,说明丙中存在Fe3+ 3Fe+4H2O(g)![]() Fe3O4+4H2 2Al+2OH-+2H2O=2AlO2-+3H2↑
Fe3O4+4H2 2Al+2OH-+2H2O=2AlO2-+3H2↑
【解析】
A、B为金属,C、D常温下是气体,且D为黄绿色气体,甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质,结合转化关系可知,甲为四氧化三铁,B为Al,A为Fe,C为氢气,乙为偏铝酸钠,丙为氯化铁,然后结合元素化合物知识及化学用语来解答。
(1)B与甲反应是铝热反应,反应的化学方程式为3Fe3O4+8Al![]() 9Fe+4Al2O3;
9Fe+4Al2O3;
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中发生钝化,金属不能溶解,
故答案为:否;
(3)检验铁离子的方法为取少量丙的溶液于试管中,滴加KSCN溶液,若溶液变红,说明丙中存在Fe3+,
故答案为:取少量丙的溶液于试管中,滴加KSCN溶液,若溶液变红,说明丙中存在Fe3+;
(4)A与水蒸气反应生成C和甲的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(5)①金属铝与NaOH溶液反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑。