题目内容
已知1g火箭燃料肼(N2H4)气体燃烧生成N2和H2O(g)时,放出16.7kJ的热量,则该反应的热化学方程式正确的是( )
| A.N2H4+O2=N2+2H2O△H= —534.4kJ/mol |
| B.N2H4(g)+ O2(g)=N2(g)+2H2O(g)△H = —16.7kJ/mol |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H = —534.4kJ/mol |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H = —534.4kJ/mol |
D
A中没有标明状态,B中反应热的数值不正确,C中水的状态不是气态,所以只有选项D是正确的,答案选D。

练习册系列答案
相关题目



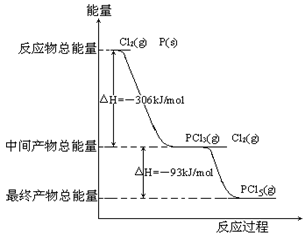
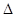 H=-
H=-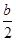 kJ/mol
kJ/mol