题目内容
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) △H=+84kJ/mol
2H2(g)+O2(g)═2H2O(g) △H=484 kJ/mol
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:________________________________
(2)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应CO(g)+2H2(g)![]() CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
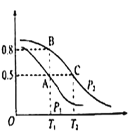
①A、B两点对应的压强大小关系是PA________PB(填“>”,“<”,“=”)
②A、B、C三点的平衡常数KA、KB、KC的大小关系是 ___________
③下列叙述能说明上述反应能达到化学平衡状态的是___(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
(3)在P1压强、T1℃时,该反应的平衡常数K=_________,再加入1.0molCO后重新到达平衡,则CO的转化率___________(填“增大”、“不变”或“减小”)
(4)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol H2:0.2mol CH3OH:0.2mol。此时v正 ________ v逆(填>、< 或 =)。
【答案】2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g) △H=-316kJ/mol < KA=KB>KC b 100 减小 >
【解析】
(1)已知:①CH3OH(g)=HCHO(g)+H2(g) △H=+84kJ/mol;
②2H2(g)+O2(g)=2H2O(g)△H=-484kJ/mol,将2×①+②得到CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式为2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g)△H=-316kJ/mol;
(2)①反应CO(g)+2H2(g)![]() CH3OH(g)是气体体积减小的反应,增大压强,平衡正向移动,反应物转化率增大,所以PA<PB;
CH3OH(g)是气体体积减小的反应,增大压强,平衡正向移动,反应物转化率增大,所以PA<PB;
②据图分析,随温度升高CO转化率降低,说明正反应放热,升温平衡逆向移动,平衡常数减小,所以KA=KB>KC;
③a.H2的消耗速率是CH3OH生成速率的2倍,二者表示的都是正反应速率,因此不能说明反应是否达到平衡状态,a错误;
b.CH3OH的体积分数不再改变说明正逆反应速率相等,反应达到平衡状态,b正确;
c.容器体积和气体质量始终不变,所以混合气体的密度始终不变,因此不能根据密度不变判断反应是否达到平衡状态,c错误;
d.CO和甲醇的化学计量数都为1,所以CO和CH3OH的物质的量之和始终保持不变,因此不能这一点判断反应是否达到平衡状态,d错误;
故合理选项是b;
(3)P1压强、T1°C时CO的转化率为0.5,
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始浓度(mol/L) 0.1 0.2 0
改变浓度(mol/L) 0.050.1 0.05
平衡浓度(mol/L) 0.050.1 0.05
化学平衡常数K=![]() ;
;
若温度不变,再加入1.0molCO,平衡向正反应移动,重新达到平衡,氢气的转化率增大,但CO投入量大于平衡移动转化量,所以CO的转化率减小;
(4) T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol H2:0.2mol CH3OH:0.2mol,此时反应的浓度商Qc=![]() <100,此时反应正向进行v正>v逆。
<100,此时反应正向进行v正>v逆。

【题目】锰元素在多个领域中均有重要应用,回答下列问题。
(1)Mn在元素周期表中位于_____区;MnSO4中阳离子的价电子排布式为__________;
(2)Mn3+在水溶液中容易歧化为MnO2和Mn2+下列说法合理的是_______
A.Mn3+的价电子构型为3d4,不属于较稳定的电子构型
B.根据Mn2+的电子构型可知,Mn4+中不含成对电子
C.Mn2+易被氧化,可能是因为Mn2+产内有大量自旋方向相同的电子
D.Mn2+与Fe3+具有相同的价电子构型,所以它们的化学性质相似
(3)在K2MnF6中,MnF62-的空间构型是正八面体,则中心原子的价层电子对数为_____。该化合物中含有的共价键在形成过程中原子轨道的重叠方式为__________
(4)二价锰的化合物的性质如下表所示:
物质 | MCl2 | MnS | MnSO4 |
熔点 | 650℃ | 1610℃ | 700℃ |
上表三种物质中晶格能最大的是________;上表涉及的三种阴离子中,半径最大的是______。
(5)某锰氧化物的晶胞结构如下图所示:

该锰的氧化物的化学式为______________,该晶体中Mn的配位数为____________,该晶体中Mn之间的最近距离为____________pm(用a、b来表示)。
【题目】回收的废旧锌锰干电池经过处理后可得到锰粉(含MnO2、Mn(OH)2、Fe和炭粉等),由锰粉为主要原料制备高性能磁性材料碳酸锰(MnCO3)的工艺流程如下:
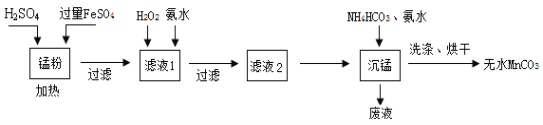
已知:①2H2SO4 + MnO2 + 2FeSO4 = MnSO4 + Fe2(SO4)3 + 2H2O
②部分氢氧化物的Ksp(近似值)如下表(25 ℃)
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp | 10-13 | 10-17 | 10-38 |
根据上图流程及有关数据回答下列问题。
(1)锰粉酸溶时,过量FeSO4所起的作用为______________________。
(2)往滤液1中先加入H2O2的目的是氧化Fe2+,该反应的离子方程式为________________,后加入氨水的目的是调节pH除去杂质离子,使滤液中的杂质离子沉淀完全(残留在溶液中的离子浓度≤ l0-5 mol·L-1),常温下测得溶液中c(Mn2+)=0.1 mol·L-1,则需调节溶液的pH范围为_______________。
(3)沉锰工序中,加入氨水的目的是(从化学平衡移动的角度解释)___________,沉锰工序中判断沉淀已经洗涤干净的实验操作是________________________________。
(4)沉锰后废液中的主要成份为_____________________________。