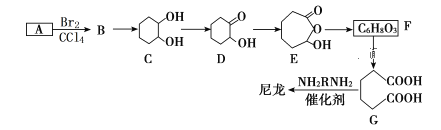
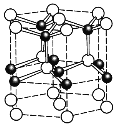
��Ŀ����
����Ŀ������(�Ҷ���)��������Ȼ���ֲ���У���������κͼ���������ˮ���������������ˮ�����ᾧ��(H2C2O4��2H2O)��ɫ���۵�Ϊ101�棬������ˮ����������ˮ��������175��ʱ�ֽ⡣
��.�������������Ʊ����ᾧ�岢�ⶨ�䴿�ȣ��Ʊ�װ����ͼ��ʾ(���ȡ��̶���װ����ȥ)��ʵ�鲽������
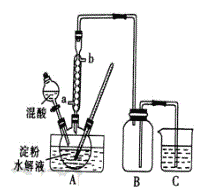
���ǻ����Ƚ�����ˮ��Ϊ�����ǣ�
���������ڵ���ˮ��Һ�м������(����֮��Ϊ3��2��65%HNO3��98%H2SO4�Ļ����)����55��60����ˮԡ���ȷ�����Ӧ��
�۽ᾧ�������������Ӧ����Һ����ȴ����ѹ���ˣ����ò��ᾧ��ֲ�Ʒ��
(1)װ�������������Ϊ__________��������У�ˮԡ���ȵ��ŵ�Ϊ___________��
(2)����������ʱ��������Ҫ��Ӧ���£�������л�ѧ����ʽ��_____C6H12O6+______HNO3![]() ______H2C2O4+9NO2��+3NO��+_________
______H2C2O4+9NO2��+3NO��+_________
(3)��ȡm g���ᾧ��ֲ�Ʒ�����100 mL��Һ��ȡ20.00 mL����ƿ�У���a mol/LKMnO4��Һ�ζ���ֻ����5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O��Ӧ������KMnO4��Һ���ΪV mL�������ò��ᾧ��(H2C2O4��2H2O)�Ĵ���Ϊ_________��
��.֤�����ᾧ��ֽ�õ��IJ���
(4)��ͬѧѡ���Ҳ�װ����֤����CO2��װ��B����Ҫ������_______________��
(5)��ͬѧ��Ϊ���ᾧ��ֽ�IJ����г���CO2��H2OӦ�û���CO��Ϊ��֤�Ƿ���CO��ѡ�ü�ͬѧʵ���е�װ��A��B����ͼ��ʾ�IJ���װ��(�����ظ�ѡ��)����ʵ�顣
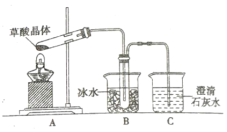




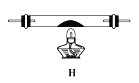
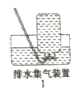
����ͬѧ��ʵ��װ���У��������ӵĺ���˳��ΪA��B��_________������װ��H��Ӧ����ʢ�е�������_____________��(д��ѧʽ)
����֤�����ᾧ��ֽ��������CO��������______________��
���𰸡���Һ©�� ���Ⱦ��ȣ����ڿ����¶� 1 12 3 9H2O ![]() ��100% ʹ�����IJ��������������CO2����ĸ��� F��D��G��H��D��I CuO H�ں�ɫ������ɫ����һ��Dװ�������ڶ���Dװ�ó��ְ�ɫ���ǣ�����֤�������к���CO��
��100% ʹ�����IJ��������������CO2����ĸ��� F��D��G��H��D��I CuO H�ں�ɫ������ɫ����һ��Dװ�������ڶ���Dװ�ó��ְ�ɫ���ǣ�����֤�������к���CO��
��������
��(1)װ����װ�����Ϊ��Һ©����ˮԡ�����Ƿ�Ӧ�¶ȵ���100������������Ⱦ��ȣ����ڿ��ƣ�
(2)����������ʱ��������Ҫ��Ӧ����ϵ����غ��ԭ���غ���ƽ��ѧ����ʽ��
(3)��Ҫ��������CO���ڼ���ʵ�����Ũ�������Ƴ�ȥ������̼���ó���ʯ��ˮ����CO2���ü�ʯ�Ҹ���CO������CO�Ļ�ԭ�Խ�CO�����������ó���ʯ��ˮ�������ɵ�CO2������ˮ���ռ�CO��Hװ����ʢ�ŵ�����Ӧ�þ��������ԣ��Һ�CO��Ӧ��������������
��CO���л�ԭ�ԣ������������Ƕ�����̼��������̼��ʹ����ʯ��ˮ����ǣ�
��(4)Bװ���¶Ƚϵͣ����������ã���ֹ����ʵ�飻
(5)��Ҫ��������CO���ڼ���ʵ�����Ũ�������Ƴ�ȥCO2���ó���ʯ��ˮ����CO2���ü�ʯ�Ҹ���CO������CO�Ļ�ԭ�Խ�CO�����������ó���ʯ��ˮ�������ɵ�CO2������ˮ���ռ�CO��Hװ����ʢ�ŵ�����Ӧ�þ��������ԣ��Һ�CO��Ӧ��������������
��CO���л�ԭ�ԣ�������������CO2��CO2��ʹ����ʯ��ˮ����ǡ�
��(1)����ͼʾ��֪װ�������������Ϊ��Һ©����ˮԡ���ȵ��ŵ�Ϊ��ʹ���Ⱦ��ȣ����ڿ����¶ȣ�
(2)��Ӧ��̼Ԫ�ػ��ϼ��ɷ�ӦǰC6H12O6�е�0������ΪH2C2O4�е�+3�ۣ�����ת��3��6=18����Ԫ�ػ��ϼ��з�ӦǰHNO3�е�+5�۽��͵�NO2�е�+4�ۣ�����ת��1�������͵�NO�е�+2�۵���ת��3������ϻ�ѧ����ʽ��NO2ϵ����9��NOϵ����3����֪�õ���������Ϊ��1��9+3��3=18�����ʸ���Nԭ���غ��֪HNO3ϵ����12��������ϵ����1��H2C2O4ϵ����3��Ȼ�����Hԭ���غ㣬��֪ȱ��������H2O��ϵ����9������ƽ�Ļ�ѧ����ʽ��C6H12O6+12HNO3��3H2C2O4+9NO2��+3NO��+9H2O��
(3)��ȡm g���ᾧ��ֲ�Ʒ�����100 mL��Һ��ȡ20.00 mL����ƿ�У���a moL/LKMnO4��Һ�궨��ֻ����5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O��Ӧ������KMnO4��Һ���ΪV mL����Ӧ����KMnO4�����ʵ�����n(KMnO4)= a moL/��V��10-3 L=aV��10-3 mol�����ݷ���ʽ��֪���ʷ�Ӧʱ��n(H2C2O4)��n(KMnO4)=5��2����20.00 mL��Һ�к��в�������ʵ���Ϊn(H2C2O4)=![]() n(H2C2O4)=
n(H2C2O4)=![]() ��aV��10-3 mol����100 mL��Һ�к��������ʵ���n(H2C2O4)��=
��aV��10-3 mol����100 mL��Һ�к��������ʵ���n(H2C2O4)��=![]() ��aV��10-3 mol��
��aV��10-3 mol��![]() =1.25aV��10-2 mol�������ò��ᾧ��(H2C2O42H2O)�Ĵ���=
=1.25aV��10-2 mol�������ò��ᾧ��(H2C2O42H2O)�Ĵ���=![]() ��100%=
��100%=![]() ��100%��
��100%��
��(4)�����ӷ����������ɵ������к��в��ᣬ������������Ʒ�Ӧ���������ԵIJ���ƶ�����CO2�ļ��飬Bװ���¶Ƚϵͣ�ʹ�����IJ�����������ֹ����CO2�ļ��飻
(5)��Ҫ��������CO���ڼ���ʵ�����ŨNaOH��Һ��ȥCO2���ó���ʯ��ˮ����CO2���ü�ʯ�Ҹ���CO
��CO���л�ԭ�ԣ�������������CO2��CO2��ʹ����ʯ��ˮ����ǣ���CO����ɫ��CuO��ԭΪ��ɫ��Cu��ֻҪH�к�ɫ����ת��Ϊ��ɫ�ҵ�һ��Dװ�������ڶ���Dװ�ó��ְ�ɫ���Ǿ�˵������CO��

 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�