题目内容
有FeO、Fe2O3的混合物若干克,在足量H2气流中,加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g;将等质量的原混合物与盐酸反应,欲使之完全溶解,需1mol?L﹣1的盐酸的体积至少为( )
| A.0.05 L | B.0.1 L | C.0.2 L | D.1 L |
B.
解析试题分析:FeO、Fe2O3的混合物,在足量H2气流中,加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g为混合物中氧原子的质量,物质的量 =0.05mol;将等质量的FeO、Fe2O3的混合物与盐酸反应,使之完全溶解,当恰好反应时,需要盐酸的体积最小,此时恰好为FeCl2、FeCl3,FeO、Fe2O3中O元素为﹣2价,用﹣1价的Cl﹣替换﹣2价的O,所以n(Cl﹣)=2n(O)=0.05mol×2=0.1mol,所以盐酸的体积为
=0.05mol;将等质量的FeO、Fe2O3的混合物与盐酸反应,使之完全溶解,当恰好反应时,需要盐酸的体积最小,此时恰好为FeCl2、FeCl3,FeO、Fe2O3中O元素为﹣2价,用﹣1价的Cl﹣替换﹣2价的O,所以n(Cl﹣)=2n(O)=0.05mol×2=0.1mol,所以盐酸的体积为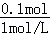 =0.1L.
=0.1L.
考点:有关混合物反应的计算.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.常温常压下,17g甲基(—14CH3)所含的中子数为9NA |
| B.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| C.42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| D.5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA |
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,22.4LCCl4含有NA个分子 |
| B.常温常压下46gNO2和N2O4混合气体含有3NA个原子 |
| C.0.1molAlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子 |
| D.0.1molCl2与足量NaOH溶液反应,转移电子数为0.2 NA |
当0.2molNa218O2足量CO2完全反应后所得固体的质量为( )
| A.21.2g | B.21.6g | C.22.0g | D.22.4g |
能正确表示下列反应的化学方程式是
A.黄铁矿煅烧:2FeS2+5O2  2FeO+4SO2 2FeO+4SO2 |
B.石英与石灰石共熔:SiO2+CaO CaSiO3 CaSiO3 |
C.氨的催化氧化:4NH3+5O2  4NO+6H2O 4NO+6H2O |
| D.氯气与石灰乳反应:2Cl2+2Ca(OH)2=CaCl3+CaClO2+2H2O |
下列化学用语正确的是( )
| A.CaH2的电子式:[H:]_Ca2+[:H]- | B.铝离子的结构示意图: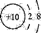 |
C.CO2的比例模型: | D.核内有8个中子的碳原子: |
下列有关化学用语使用正确的是( )
A.CO2的电子式: |
| B.次氯酸的结构式: H—O—Cl |
C.中子数为18的氯原子结构示意图: |
| D.二氧化硅的分子式为:SiO2 |
下列各项表达中正确的是
A.乙烯的电子式: |
B.羟基的电子式为: |
C.甘油的结构简式: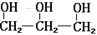 |
| D.苯酚分子式:C6H5OH |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2L的水中含有0.5个NA水分子 |
| B.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Mg2+的个数为0.5NA |
| C.1 mol H2和O2的混合气体中含NA个分子 |
| D.11.2L NH3中所含的原子数目为2NA |