题目内容
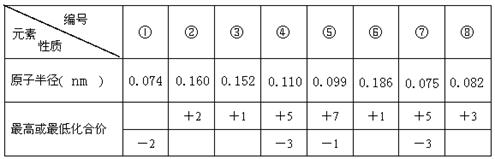
现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
回答下列问题:
(1)①在元素周期表中的位置是(周期、族) ;
(2)比较④和⑦的氢化物的稳定性(用化学式表示) 。

回答下列问题:
(1)①在元素周期表中的位置是(周期、族) ;
(2)比较④和⑦的氢化物的稳定性(用化学式表示) 。
(4分)(1)第二周期第Ⅵ A族;(2分)(2)NH3>PH3(2分)
试题分析:电子层越多,半径越大,同周期从左向右原子半径在减小,最高正价在增大,最高正价等于族序数,由短周期元素的数据可知,①为O,②为Mg,③为Li,④为P,⑤为Cl,⑥为Na,⑦为N,⑧为B,
(1)①为O,在元素周期表中的位置是第二周期第Ⅵ A族。
(2)④⑦同主族,④的原子半径大,则原子序数大,④和⑦的氢化物的稳定性是NH3>PH3。考点:
点评:本题考查原子结构与元素周期律,熟悉原子半径、化合价的变化规律是解答本题的关键,题目难度不大,⑧为学生解答的易错点。

练习册系列答案
相关题目
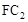 气体有毒,排放到大气中易形成酸雨,写出
气体有毒,排放到大气中易形成酸雨,写出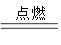 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)