题目内容
在一定条件下,NO与NO2混合可生成N2O3,反应的化学方程式为:NO(g)+NO2(g) N2O3(g) ΔH<0
N2O3(g) ΔH<0
下图表示一定量的NO、NO2混合气体发生反应时,NO2浓度在前25s内的变化。该反应进行到45s时达到平衡,测得NO2浓度约为0.010mol/L。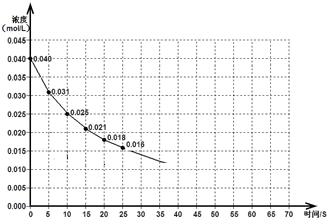
(1)前20s内,NO2的平均反应速率为_________________。
(2)其他条件不变,①升高温度,NO2的转化率_______ (填“增大”、“减小”或“不变”)。
②压缩气体体积,该反应平衡向_______移动(填“正向”或“逆向”)。
(3)若反应延续至70秒,请在答题卡图中画出25秒至70秒的反应进程曲线。
(4)若在反应开始时加入催化剂(其他条件都不变),请在答题卡图中画出加催化剂后的反应进程曲线。
(5)NO、NO2的混合气体用NaOH溶液吸收,得到的盐只有一种,则该反应的离子方程式为:___________________________________,该反应的氧化剂是______________。
(16分)
(1)1.1×10-3 mol·L-1·s-1(3分,单位、有效数字错漏合扣1分)
(2)①减小(2分) ②正向(2分)
(3)、(4)(如图,各2分,共4分,注意曲线起点、斜率、平衡点要素有错,每个要素扣1分直至0分,使用催化剂不标注扣1分)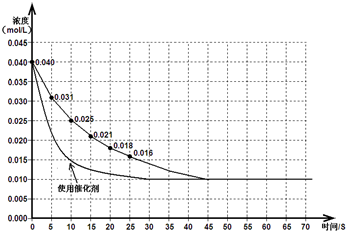
(5)NO + NO2 + 2OH-=2NO2-+ H2O(3分); NO2(2分)
解析试题分析:(1)起始时、20s时二氧化氮浓度分别为0.040 mol·L-1、0.018 mol·L-1,则前20s内二氧化氮的平均反应速率=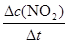 =
=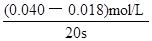 =1.1×10-3mol/(L?s);(2)①ΔH<0,说明正反应是放热反应,升高温度平衡向吸热反应或逆反应方向移动,则二氧化氮的平衡转化率减小;②NO(g)+NO2(g)
=1.1×10-3mol/(L?s);(2)①ΔH<0,说明正反应是放热反应,升高温度平衡向吸热反应或逆反应方向移动,则二氧化氮的平衡转化率减小;②NO(g)+NO2(g) N2O3(g)的正反应是气体体积减小的反应,压缩容器的体积就是增大压强,使平衡向气体体积减小方向或正反应方向移动;(3)依题意,该反应达到平衡的时间是45s,则25s~45s,二氧化氮的浓度由0.018mol/L逐渐减小至0.010mol/L,45s~70s二氧化氮的浓度保持不变;(4)画图要点:①催化剂能加快反应速率,缩短达到平衡的时间,因此达到平衡的时间小于45s;②催化剂对平衡移动无影响,加入催化剂不能使平衡移动,则平衡时及平衡后二氧化氮的浓度为0.010mol/L;(5)依题意,等物质的量的NO与NO2反应生成N2O3,N2O3溶于水时得到亚硝酸,HNO2与NaOH发生中和反应,生成亚硝酸钠和水,由此推断混合气体溶于氢氧化钠溶液的原理为:NO + NO2 + 2OH-=2NO2-+ H2O;该反应中NO是还原剂,所含氮元素由+2升为+3价,而NO2是氧化剂,所含氮元素由+4降为+2价。
N2O3(g)的正反应是气体体积减小的反应,压缩容器的体积就是增大压强,使平衡向气体体积减小方向或正反应方向移动;(3)依题意,该反应达到平衡的时间是45s,则25s~45s,二氧化氮的浓度由0.018mol/L逐渐减小至0.010mol/L,45s~70s二氧化氮的浓度保持不变;(4)画图要点:①催化剂能加快反应速率,缩短达到平衡的时间,因此达到平衡的时间小于45s;②催化剂对平衡移动无影响,加入催化剂不能使平衡移动,则平衡时及平衡后二氧化氮的浓度为0.010mol/L;(5)依题意,等物质的量的NO与NO2反应生成N2O3,N2O3溶于水时得到亚硝酸,HNO2与NaOH发生中和反应,生成亚硝酸钠和水,由此推断混合气体溶于氢氧化钠溶液的原理为:NO + NO2 + 2OH-=2NO2-+ H2O;该反应中NO是还原剂,所含氮元素由+2升为+3价,而NO2是氧化剂,所含氮元素由+4降为+2价。
考点:考查化学反应原理,涉及反应物的浓度—时间图像、平均反应速率的计算、外界条件对平衡移动的影响、画反应物浓度随时间变化示意图、催化剂对反应速率和平衡移动的影响、离子方程式、氧化还原反应中的氧化剂等。

甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |
(1)反应②是 (填“吸热”或“放热”)反应。
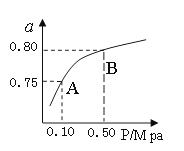
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是 。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是 。
(4)甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼 雷电池,其原理如图所示。该电池的负极反应式是

(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为 。
 2NH3(g)反应的影响,实验结果可表示成如图所示的规律(图中T表示温度,n表示物质的量):
2NH3(g)反应的影响,实验结果可表示成如图所示的规律(图中T表示温度,n表示物质的量):

 4NO+6H2O ,4NH3+3O2
4NO+6H2O ,4NH3+3O2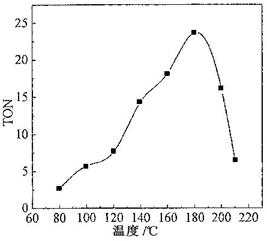
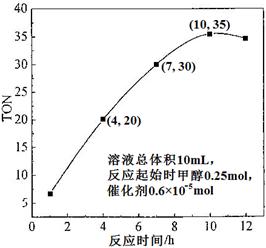
 Si3N4(s) + 6CO(g) + Q(Q>0)
Si3N4(s) + 6CO(g) + Q(Q>0)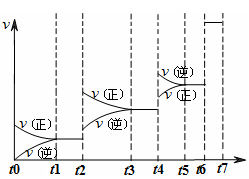
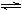 NH3(g) + HI(g)
NH3(g) + HI(g)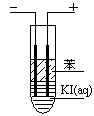
 H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
 2CO (g)平衡常数K1;
2CO (g)平衡常数K1; CO(g) +H2 (g)平衡常数K2则K、K1、K2,之间的关系是 :
CO(g) +H2 (g)平衡常数K2则K、K1、K2,之间的关系是 : 2CrO42- + 2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
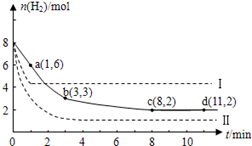
2CrO42- + 2H+,把K2Cr2O7溶于水配成稀溶液是橙色。 CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.
CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.